Тип кислотно-основного титрування: Сильна кислота + сильна основа. Крива титрування.
Візьмемо найпоширеніші індикатори кислотно-основного титрування:
Метиловий-помаранчовий, інтервал рН зміни кольору 3,50-4,40;
Метиловий-червоний 4,4-6,2;
Лакмус, інтервал рН зміни кольору 5,00-8,00;
Фенолфталеїн, інтервал рН зміни кольору 8,20-10,0.
10 мл Розчин HCl + 20 мл Розчин NaOH.
У конічній колбі знаходиться 10 мл 0,01 М розчину HCl. Починаємо додавати із бюретки 0,01 M розчин NaOH. Що відбувається?
Концентрація хлоридної кислоти знижується внаслідок реакції з натрій гідроксідом, та внаслідок збільшення об'єму розчину. Тобто для розрахунку рН після додавання кожної новой порції титранту треба врахувати реакцію нейтралізації, та збільшення об'єму розчину. Вплив сольватації та іонну силу розчину не враховуємо.
Використовуємо MatLab (демо-версія звісно) для автоматизації розрахунків, та прослідковування зміни рН розчину в процесі титрування, якщо порція титранту дорівнюватиме 0,02 мл - 1 крапля з бюретки.
Програма для розрахунку MatLab
Код: Виділити все
x1=0:0.02:9.9999;
x2=10.0001:0.02:20;
c1 = (0.1-0.01*x1)./(10+x1);
y1 = -log10(c1);
c2 = ((0.1-0.01*x2)./(10+x2)).*-1;
y2 = -log10(1e-14./c2);
x=cat(2,x1,x2);
y=cat(2,y1,y2);
plot(x,y,'-')
axis([0 20 0 12])
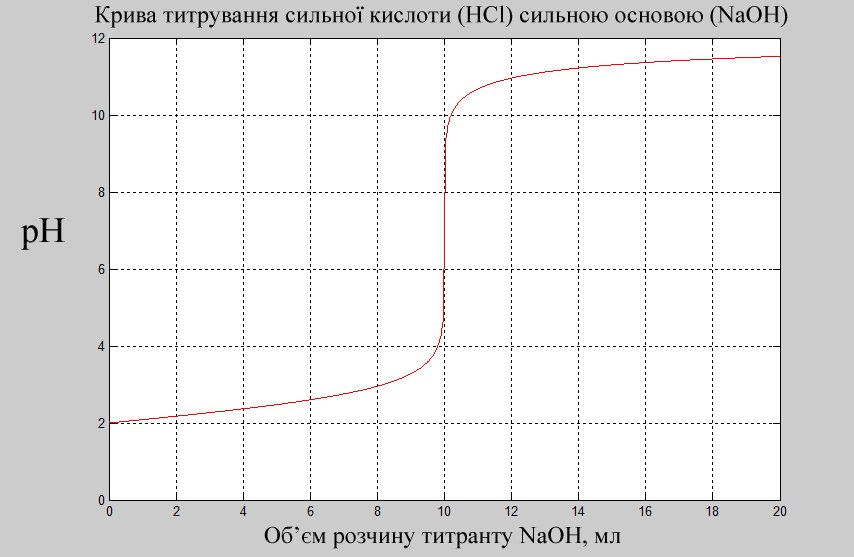
grid onІнтервал стрибка рН в точці еквівалентності з рН=4 до рН=10.
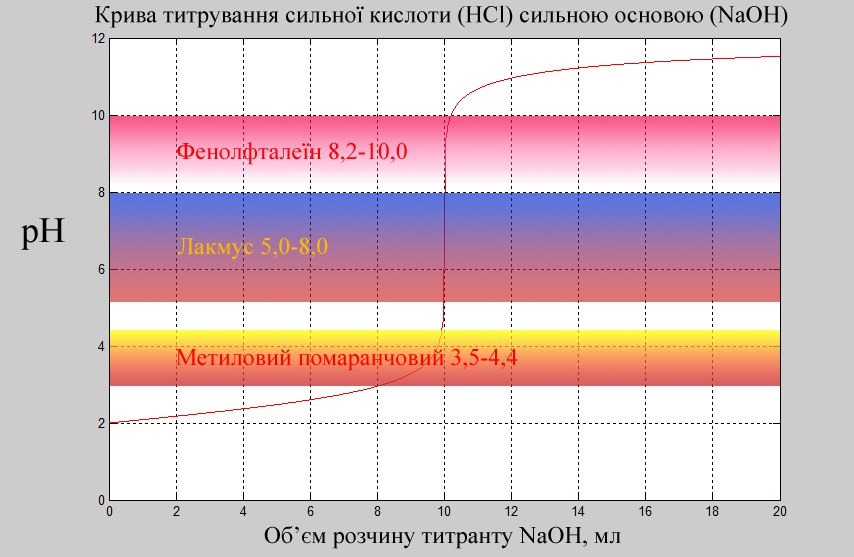
Показник титрування трьох основних індикаторів знаходиться в межах стрибка. Отже для титрування сильної кислоти сильною основою підійдуть всі наведені індикатори, а найточнішим буде титрування з індикатором Лакмус.
Тип кислотно-основного титрування: слабка кислота + сильна основа. Крива титрування.
Якщо титрувати слабку кислоту сильною основою, утворюється сіль слабкої кислоти та сильної основи, яка при гідролізі дає лужне середовище. Органічні кислоти в фруктах є слабкими кислотами. При визначенні кислотності фруктів велике значення має правильний вибір індикатору, який використовують в процесі титрування.
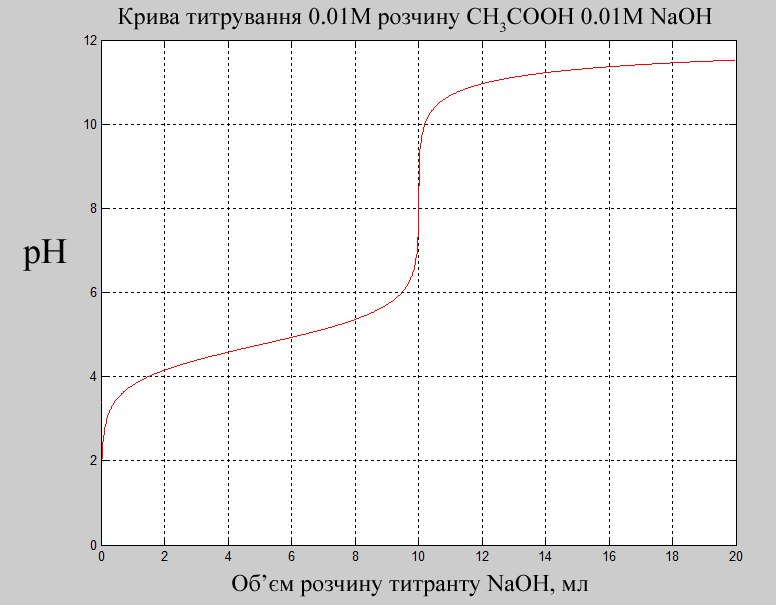
Побудуємо криву титрування 0,01М розчину оцтової кислоти, 0,01М розчином натрій гідроксиду. Значення рН стрибка у точці еквівалентності знаходиться в межах від 7,0 до 10,0. Порівнюючи інтервал переходу кольору різних індикаторів, бачимо, що метиловий-помаранчовий (3,5-4,4) знаходиться за межами стрибка рН, лакмус (5-8) захоплює точку еквівалентності тільки переходом у синій колір, а фенолфталеїн знаходиться в потрібному інтервалі рН.
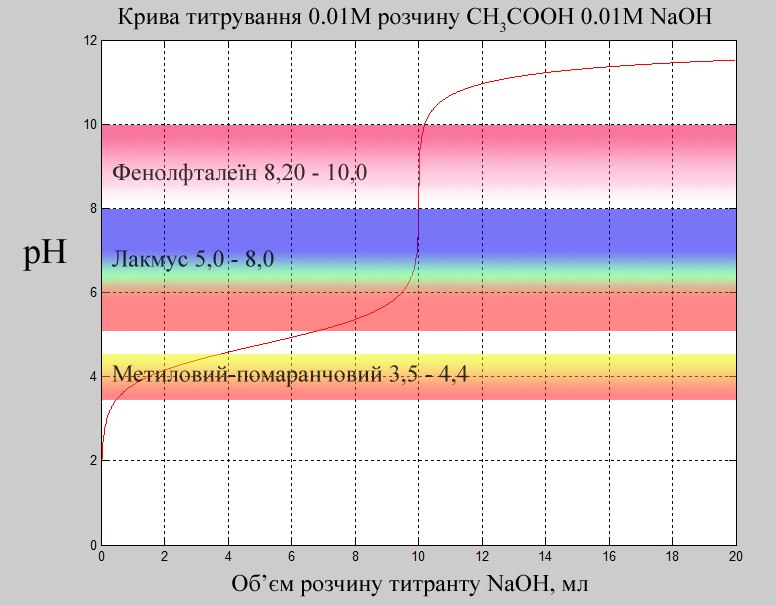
Отже, використовуючи лакмус, будемо спостерігати поступову зміну забарвлення розчину від червоного до зеленуватого, а потім, у точці еквівалентності різке виникнення синього кольору.
Фенолфталеїн покаже різку зміну від безбарвного до малинового у точці еквівалентності. Саме фенолфталеїн найбільше підходить для титрування розчину слабкої кислоти сильною основою.
Тип кислотно-основного титрування: сильна кислота + слабка основа. Крива титрування.
Розрахунок рН для кривої титрування: Титрування 10 мл 0,01М розчину амоній гідроксиду, 0,01М розчином хлоридної кислоти.
В результаті хімічної реакції утворюється сіль слабкої основи та сильної кислоти, яка при гідролізі дає кисле середовище.
Який індикатор обрати для титрування в цьому випадку? Побудуємо криву титрування:
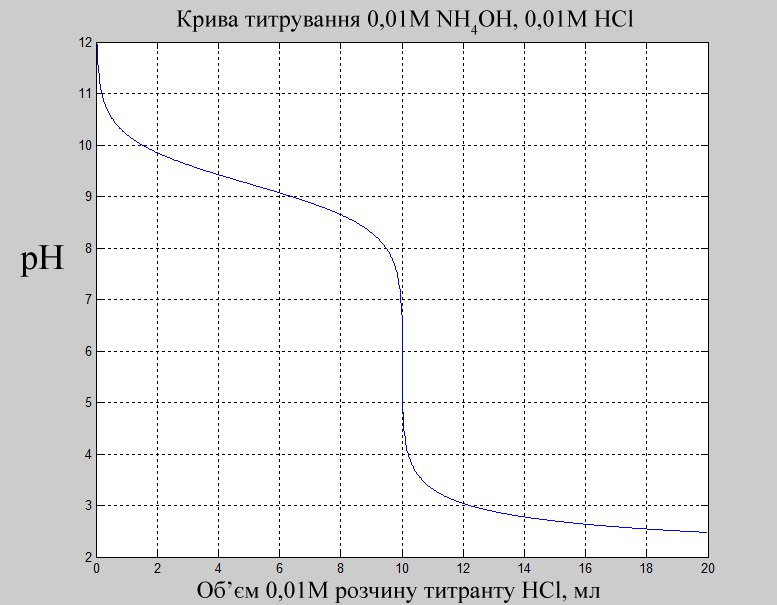
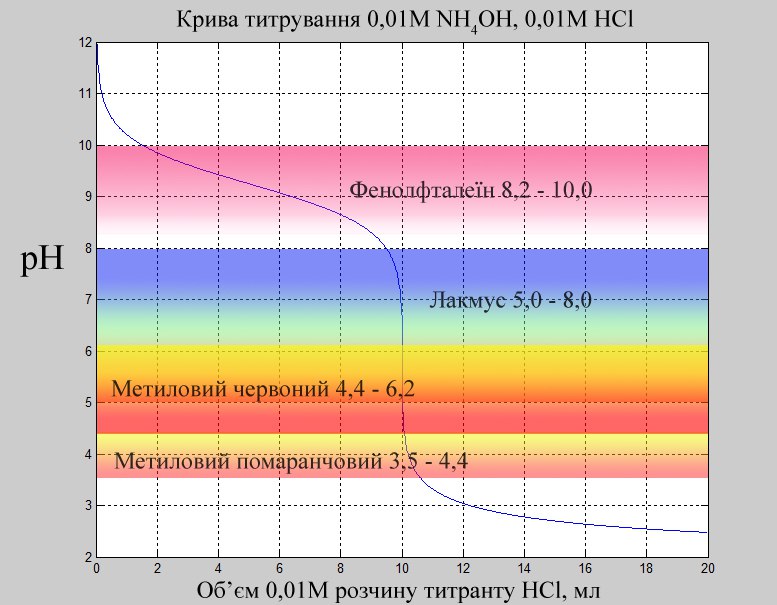
Стрибок рН у точці еквівалентності від 4,5 до 7,5.
Фенолфталеїн та метиловий-помаранчовий знаходяться за межами стрибка рН.
Для титрування підійтуть індикатори лакмус та метиловий-червоний (4,4-6,2). Найкраще підходить метиловий-червоний, в точці еквівалентності його колір різко змінеться з жовтого на червоний.