ąĄąĮčéą░ą╗čīą┐č¢čÅ čĆąĄą░ą║čåč¢čŚ – čåąĄ čĆč¢ąĘąĮąĖčåčÅ ą╝č¢ąČ čüčāą╝ąŠčÄ ąĄąĮčéą░ą╗čīą┐č¢ą╣ čāčéą▓ąŠčĆąĄąĮąĮčÅ ą┐čĆąŠą┤čāą║čéč¢ą▓ čĆąĄą░ą║čåč¢čŚ čéą░ čüčāą╝ąŠčÄ ąĄąĮčéą░ą╗čīą┐č¢ą╣ čāčéą▓ąŠčĆąĄąĮąĮčÅ čĆąĄą░ą│ąĄąĮčéč¢ą▓ ąĘ čāčĆą░čģčāą▓ą░ąĮąĮčÅą╝ čüč鹥čģč¢ąŠą╝ąĄčéčĆąĖčćąĮąĖčģ ą║č¢ą╗čīą║ąŠčüč鹥ą╣ čĆąĄč湊ą▓ąĖąĮ
╬öH = ╬Ż (n╬öH)ą┐čĆąŠą┤čāą║čéąĖ – ╬Ż (n╬öH)čĆąĄą░ą│ąĄąĮčéąĖ
ąöą╗čÅ ą┤ąĄčÅą║ąŠčŚ čĆąĄą░ą║čåč¢čŚ:
nAA + nBB = nCC + nDD
čüčéą░ąĮą┤ą░čĆčéąĮą░ ąĄąĮčéą░ą╗čīą┐č¢čÅ čĆąĄą░ą║čåč¢čŚ ą┤ąŠčĆč¢ą▓ąĮčÄčö:
╬öH┬░298 = (nC╬öH┬░298(ąĪ) + nD╬öH┬░298(D)) – (nA╬öH┬░298(A) + nB╬öH┬░298(B))
ą¤čĆąĖą║ą╗ą░ą┤. ąĪčéą░ąĮą┤ą░čĆčéąĮą░ ąĄąĮčéą░ą╗čīą┐č¢čÅ ąĮą░čüčéčāą┐ąĮąŠčŚ čĆąĄą░ą║čåč¢čŚ:
4NH3 (ą│)+ 5O2 (ą│) = 4NO(ą│) + 6H2O(ą│)
╬öH┬░298 = (nNO ┬Ę ╬öH┬░298(NO) + nH2O ┬Ę ╬öH┬░298(H2O)) – (nNH3┬Ę ╬öH┬░298(NH3) + n O2┬Ę ╬öH┬░298(O2)) =
= (4┬Ę(+91) + 6┬Ę(- 242)) – (4┬Ę(-46) + 5┬Ę(0)) = -904 ą║ąöąČ
ąĀąŠąĘą┤č¢ą╗ čģč¢ą╝č¢čŚ, čÅą║ąĖą╣ ą┐čĆąĖčüą▓čÅč湥ąĮąĖą╣ ą║č¢ą╗čīą║č¢čüąĮąŠą╝čā ą▓ąĖąĘąĮą░č湥ąĮąĮčÄ č鹥ą┐ą╗ąŠą▓ąĖčģ ąĄč乥ą║čéč¢ą▓ čģč¢ą╝č¢čćąĮąĖčģ čĆąĄą░ą║čåč¢ą╣, ąĮą░ąĘąĖą▓ą░čöčéčīčüčÅ č鹥čĆą╝ąŠčģč¢ą╝č¢čÅ.
 ąĀąŠąĘčĆą░čģčāąĮąŠą║ č鹥ą┐ą╗ąŠą▓ąĖčģ ąĄč乥ą║čéč¢ą▓ čĆąĄą░ą║čåč¢ą╣, ąĘąŠą║čĆąĄą╝ą░ ą┐čĆąĖ p = const, ąĘą░čüąĮąŠą▓ą░ąĮąĖą╣ ąĮą░ ą┤ą▓ąŠčģ ąĘą░ą║ąŠąĮą░čģ č鹥čĆą╝ąŠčģč¢ą╝č¢čŚ.
ąĀąŠąĘčĆą░čģčāąĮąŠą║ č鹥ą┐ą╗ąŠą▓ąĖčģ ąĄč乥ą║čéč¢ą▓ čĆąĄą░ą║čåč¢ą╣, ąĘąŠą║čĆąĄą╝ą░ ą┐čĆąĖ p = const, ąĘą░čüąĮąŠą▓ą░ąĮąĖą╣ ąĮą░ ą┤ą▓ąŠčģ ąĘą░ą║ąŠąĮą░čģ č鹥čĆą╝ąŠčģč¢ą╝č¢čŚ.
ą┐ąĄčĆčłąĖą╣ ąĘą░ą║ąŠąĮ č鹥čĆą╝ąŠčģč¢ą╝č¢čŚ: ą┐čĆąĖ čĆąŠąĘą║ą╗ą░ą┤ą░ąĮąĮč¢ čüą║ą╗ą░ą┤ąĮąŠčŚ čĆąĄč湊ą▓ąĖąĮąĖ ąĮą░ ą▒č¢ą╗čīčł ą┐čĆąŠčüčéč¢ čĆąĄč湊ą▓ąĖąĮąĖ ą▓č¢ą┤ą▒čāą▓ą░čöčéčīčüčÅ ąĘą╝č¢ąĮą░ ąĄąĮčéą░ą╗čīą┐č¢čŚ, čÅą║ą░ ą┤ąŠčĆč¢ą▓ąĮčÄčö (ą░ą╗ąĄ ąĘ ą┐čĆąŠčéąĖą╗ąĄąČąĮąĖą╝ ąĘąĮą░ą║ąŠą╝) ąĘą╝č¢ąĮč¢ ąĄąĮčéą░ą╗čīą┐č¢čŚ ą┐čĆąĖ čāčéą▓ąŠčĆąĄąĮąĮč¢ čåč¢čöčŚ čĆąĄč湊ą▓ąĖąĮąĖ ąĘ čéąĖčģ čüą░ą╝ąĖčģ ą┐čĆąŠčüčéąĖčģ čĆąĄč湊ą▓ąĖąĮ
ą¤ąĄčĆčłąĖą╣ ąĘą░ą║ąŠąĮ čéečĆą╝ąŠčģč¢ą╝č¢čŚ ą▓č¢ą┤ą║čĆąĖčéąĖą╣ ą▓ ą║č¢ąĮčåč¢ XVIII čüčé. čäčĆą░ąĮčåčāąĘčīą║ąĖą╝ąĖ ą▓č湥ąĮąĖą╝ąĖ ąøą░ą▓čāą░ąĘčīčö č¢ ąøą░ą┐ą╗ą░čüąŠą╝, ą┤čĆčāą│ą░ ąĮą░ąĘą▓ą░ čåčīąŠą│ąŠ ąĘą░ą║ąŠąĮčā – ąĘą░ą║ąŠąĮ ąøą░ą▓čāą░ąĘčīčö-ąøą░ą┐ą╗ą░čüą░. ążą░ą║čéąĖčćąĮąŠ čåąĄą╣ ąĘą░ą║ąŠąĮ ą▓ąĖą┐ą╗ąĖą▓ą░čö č¢ąĘ ąĘą░ą║ąŠąĮčā ąĘą▒ąĄčĆąĄąČąĄąĮąĮčÅ ąĄąĮąĄčĆą│č¢čŚ; čüą░ą╝ąĄ ąĮą░ čåčīąŠą╝čā ąĘą░ą║ąŠąĮč¢ ąĘą░čüąĮąŠą▓ą░ąĮą░ č乊čĆą╝čāą╗ą░ ą┤ą╗čÅ čĆąŠąĘčĆą░čģčāąĮą║čā ąĄąĮčéą░ą╗čīą┐č¢čŚ čĆąĄą░ą║čåč¢čŚ ą┐ąŠ ąĄąĮčéą░ą╗čīą┐č¢čŚ čāčéą▓ąŠčĆąĄąĮąĮčÅ čĆąĄč湊ą▓ąĖąĮ čÅą║č¢ ą┐čĆąĖą╣ą╝ą░čÄčéčī čāčćą░čüčéčī čā čĆąĄą░ą║čåč¢čŚ.
 ąĢąĮčéą░ą╗čīą┐č¢čÄ čāčéą▓ąŠčĆąĄąĮąĮčÅ ą▓ąĖąĘąĮą░čćąĖčéąĖ ąĄą║čüą┐ąĄčĆąĖą╝ąĄąĮčéą░ą╗čīąĮąŠ ą╝ąŠąČąĮą░ ąĮąĄ ą┤ą╗čÅ ą▓čüč¢čģ čĆąĄč湊ą▓ąĖąĮ, č湥čĆąĄąĘ čüą║ą╗ą░ą┤ąĮč¢čüčéčī ą┐čĆąŠą▓ąĄą┤ąĄąĮąĮčÅ, ą░ą▒ąŠ ą┐čĆą░ą║čéąĖčćąĮčā ąĮąĄąĘą┤č¢ą╣čüąĮąĄąĮąĮč¢čüčéčī ą▒ą░ą│ą░čéčīąŠčģ čĆąĄą░ą║čåč¢ą╣. ąóą░ą▒ą╗ąĖčćąĮč¢ ąĘąĮą░č湥ąĮąĮčÅ ╬öH┬░298ą┤ą╗čÅ ą▒ą░ą│ą░čéčīąŠčģ čĆąĄč湊ą▓ąĖąĮ ąŠčéčĆąĖą╝ą░ąĮč¢ čĆąŠąĘčĆą░čģčāąĮą║ąŠą▓ąĖą╝ čüą┐ąŠčüąŠą▒ąŠą╝, ąĮą░ ąŠčüąĮąŠą▓č¢ ą┤čĆčāą│ąŠą│ąŠ ąĘą░ą║ąŠąĮčā č鹥čĆą╝ąŠčģč¢ą╝č¢čŚ, ą▓č¢ą┤ą║čĆąĖč鹊ą╝čā ą▓ 1840 čĆ čģč¢ą╝č¢ą║ąŠą╝ ąō.ąå. ąōąĄčüčüąŠą╝, ąĘą░ą║ąŠąĮ ąōąĄčüčüą░:
ąĢąĮčéą░ą╗čīą┐č¢čÄ čāčéą▓ąŠčĆąĄąĮąĮčÅ ą▓ąĖąĘąĮą░čćąĖčéąĖ ąĄą║čüą┐ąĄčĆąĖą╝ąĄąĮčéą░ą╗čīąĮąŠ ą╝ąŠąČąĮą░ ąĮąĄ ą┤ą╗čÅ ą▓čüč¢čģ čĆąĄč湊ą▓ąĖąĮ, č湥čĆąĄąĘ čüą║ą╗ą░ą┤ąĮč¢čüčéčī ą┐čĆąŠą▓ąĄą┤ąĄąĮąĮčÅ, ą░ą▒ąŠ ą┐čĆą░ą║čéąĖčćąĮčā ąĮąĄąĘą┤č¢ą╣čüąĮąĄąĮąĮč¢čüčéčī ą▒ą░ą│ą░čéčīąŠčģ čĆąĄą░ą║čåč¢ą╣. ąóą░ą▒ą╗ąĖčćąĮč¢ ąĘąĮą░č湥ąĮąĮčÅ ╬öH┬░298ą┤ą╗čÅ ą▒ą░ą│ą░čéčīąŠčģ čĆąĄč湊ą▓ąĖąĮ ąŠčéčĆąĖą╝ą░ąĮč¢ čĆąŠąĘčĆą░čģčāąĮą║ąŠą▓ąĖą╝ čüą┐ąŠčüąŠą▒ąŠą╝, ąĮą░ ąŠčüąĮąŠą▓č¢ ą┤čĆčāą│ąŠą│ąŠ ąĘą░ą║ąŠąĮčā č鹥čĆą╝ąŠčģč¢ą╝č¢čŚ, ą▓č¢ą┤ą║čĆąĖč鹊ą╝čā ą▓ 1840 čĆ čģč¢ą╝č¢ą║ąŠą╝ ąō.ąå. ąōąĄčüčüąŠą╝, ąĘą░ą║ąŠąĮ ąōąĄčüčüą░:
ą┤čĆčāą│ąĖą╣ ąĘą░ą║ąŠąĮ č鹥čĆą╝ąŠčģč¢ą╝č¢čŚ: čüčāą╝ą░ ąĄąĮčéą░ą╗čīą┐č¢ą╣ ą┤ą▓ąŠčģ ą░ą▒ąŠ ą▒č¢ą╗čīčłąĄ ą┐čĆąŠą╝č¢ąČąĮąĖčģ čĆąĄą░ą║čåč¢ą╣ (čüčéą░ą┤č¢ą╣) ą┐čĆąĖ ą┐ąĄčĆąĄčģąŠą┤č¢ ą▓č¢ą┤ ą┐ąŠčćą░čéą║ąŠą▓ąŠą│ąŠ čüčéą░ąĮčā ą┤ąŠ ą║č¢ąĮčåąĄą▓ąŠą│ąŠ čüčéą░ąĮčā ą┤ąŠčĆč¢ą▓ąĮčÄčö ąĄąĮčéą░ą╗čīą┐č¢čŚ čĆąĄą░ą║čåč¢čŚ, čÅą║ą░ ą▒ąĄąĘą┐ąŠčüąĄčĆąĄą┤ąĮčīąŠ ą▓ąĄą┤ąĄ ą▓č¢ą┤ ą▓ąĖčģč¢ą┤ąĮąŠą│ąŠ čüčéą░ąĮčā ą┤ąŠ ą║č¢ąĮčåąĄą▓ąŠą│ąŠ čüčéą░ąĮčā
ąóą░ą║ąĖą╝ čćąĖąĮąŠą╝, ąĄąĮčéą░ą╗čīą┐č¢čÅ čĆąĄą░ą║čåč¢čŚ ąĘą░ą╗ąĄąČąĖčéčī čéč¢ą╗čīą║ąĖ ą▓č¢ą┤ ą▓ąĖą┤čā č¢ čüčéą░ąĮčā čĆąĄą░ą│ąĄąĮčéč¢ą▓, ą░ą╗ąĄ ąĮąĄ ąĘą░ą╗ąĄąČąĖčéčī ą▓č¢ą┤ ą┐čĆąŠą╝č¢ąČąĮąĖčģ čüčéą░ąĮč¢ą▓ č¢ čłą╗čÅčģčā ą┐ąĄčĆąĄčģąŠą┤čā ą▓č¢ą┤ čĆąĄą░ą│ąĄąĮčéč¢ą▓ ą┤ąŠ ą┐čĆąŠą┤čāą║čéč¢ą▓ (čåąĄ ą┤čĆčāą│ąĄ č乊čĆą╝čāą╗čÄą▓ą░ąĮąĮčÅ ąĘą░ą║ąŠąĮčā ąōąĄčüčüą░). ąŚą░ą║ąŠąĮ ąōąĄčüčüą░ ą┤ąŠąĘą▓ąŠą╗čÅčö ąĘą▓’čÅąĘą░čéąĖ ąĄąĮčéą░ą╗čīą┐č¢ą╣ąĮč¢ ąĄč乥ą║čéąĖ ą┐čĆąŠčåąĄčüčā, čÅą║ąĖą╣ ą╝ąŠąČąĄ ą┐čĆąŠčéč¢ą║ą░čéąĖ ą▓ ąŠą┤ąĮčā ą░ą▒ąŠ ą║č¢ą╗čīą║ą░ čüčéą░ą┤č¢ą╣, č¢ čĆąŠąĘčĆą░čģčāą▓ą░čéąĖ ąĄąĮčéą░ą╗čīą┐č¢čÄ (č鹥ą┐ą╗ąŠą▓ąĖą╣ ąĄč乥ą║čé) čéč¢čöčŚ čĆąĄą░ą║čåč¢čŚ, čÅą║čā ą▓ą░ąČą║ąŠ ąĘą┤č¢ą╣čüąĮąĖčéąĖ ą░ą▒ąŠ ą┤ąŠą▓ąĄčüčéąĖ ą┤ąŠ ą║č¢ąĮčåčÅ ą┐čĆą░ą║čéąĖčćąĮąŠ.
ą¤čĆąĖą║ą╗ą░ą┤. ą¤čĆąŠčåąĄčü čāčéą▓ąŠčĆąĄąĮąĮčÅ ą║ą░čĆą▒ąŠąĮ (IV) ąŠą║čüąĖą┤čā (ą║č¢ąĮčåąĄą▓ąĖą╣ čüčéą░ąĮ) ą┐čĆąĖ čüą┐ą░ą╗čÄą▓ą░ąĮąĮč¢ ą│čĆą░čäč¢čéčā (ą┐ąŠčćą░čéą║ąŠą▓ąĖą╣ čüčéą░ąĮ) ą▓ ą║ąĖčüąĮč¢ ą╝ąŠąČąĄ ą┐čĆąŠčéč¢ą║ą░čéąĖ ą┤ą▓ąŠą╝ą░ čłą╗čÅčģą░ą╝ąĖ:
- 2C + O2 = 2CO
2CO + O2 = 2CO2 - C + O2 = CO2
ąĢą║čüą┐ąĄčĆąĖą╝ąĄąĮčéą░ą╗čīąĮąŠ ą▓ąĖąĘąĮą░čćąĖčéąĖ ąĄąĮčéą░ą╗čīą┐č¢čÄ čāčéą▓ąŠčĆąĄąĮąĮčÅ CO ąĘ ą┐ąĄčĆčłąŠčŚ čĆąĄą░ą║čåč¢čŚ ąĮąĄą╝ąŠąČą╗ąĖą▓ąŠ, ą▒ąŠ ą╣ą┤ąĄ ą┤čĆčāą│ą░ čĆąĄą░ą║čåč¢čÅ – ą┐ąĄčĆąĄčéą▓ąŠčĆąĄąĮąĮčÅ CO ą▓ CO2. ą×ą┤ąĮą░ą║ ą╝ąŠąČąĮą░ ąĄą║čüą┐ąĄčĆąĖą╝ąĄąĮčéą░ą╗čīąĮąŠ ą▓ąĖąĘąĮą░čćąĖčéąĖ ąĄąĮčéą░ą╗čīą┐č¢čÄ čĆąĄą░ą║čåč¢čŚ ą┐ąĄčĆąĄčéą▓ąŠčĆąĄąĮčī CO ą▓ CO2 čÅą║čēąŠ ąŠčéčĆąĖą╝ą░čéąĖ (čÅą║ąĖą╝-ąĮąĄą▒čāą┤čī č¢ąĮčłąĖą╝ čüą┐ąŠčüąŠą▒ąŠą╝) čćąĖčüčéąĖą╣ CO, ą░ ą┐ąŠčéč¢ą╝ ą┐ąĄčĆąĄą▓ąĄčüčéąĖ ą╣ąŠą│ąŠ ą▓ CO2 čüą┐ą░ą╗čÄą▓ą░ąĮąĮčÅą╝ ą▓ ą║ąĖčüąĮč¢. ąÜčĆč¢ą╝ č鹊ą│ąŠ, ą╗ąĄą│ą║ąŠ ąĘąĮą░čģąŠą┤ąĖčéčīčüčÅ č¢ ąĄąĮčéą░ą╗čīą┐č¢čÅ ą┐ąŠą▓ąĮąŠą│ąŠ ąĘą│ąŠčĆčÅąĮąĮčÅ ą│čĆą░čäč¢čéčā (čłą╗čÅčģ 2), č鹊ą▒č鹊 ąĄąĮčéą░ą╗čīą┐č¢čÅ čāčéą▓ąŠčĆąĄąĮąĮčÅ CO2. ąŚą▓č¢ą┤čüąĖ ąĮą░ ąŠčüąĮąŠą▓č¢ ąĘą░ą║ąŠąĮčā ąōąĄčüčüą░ ą╗ąĄą│ą║ąŠ čĆąŠąĘčĆą░čģčāą▓ą░čéąĖ ąĄąĮčéą░ą╗čīą┐č¢čÄ ą┐ąĄčĆąĄčģąŠą┤čā ą│čĆą░čäč¢čéčā ą▓ CO, ą▓ąĖą║ąŠčĆąĖčüč鹊ą▓čāčÄčćąĖ čüčģąĄą╝čā:
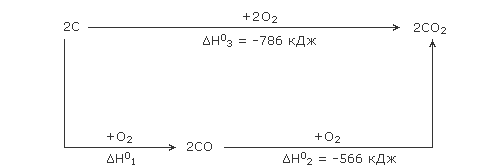
ąŚą░ ąĘą░ą║ąŠąĮąŠą╝ ąōąĄčüčüą░ ╬öH┬░1+ ╬öH┬░2 = ╬öH┬░3; ąŠčéąČąĄ:
╬öH┬░(CO) = ╬öH┬░1┬Ā/ n (CO) = (╬öH┬░3 – ╬öH┬░2) / n (CO) = ((-786 ) – (-566)) / 2 = -110 ą║ąöąČ/ą╝ąŠą╗čī
ą×čéčĆąĖą╝ą░ąĮąĄ ąĘąĮą░č湥ąĮąĮčÅ č鹊čćąĮąŠ ą▓č¢ą┤ą┐ąŠą▓č¢ą┤ą░čö ą┤ąŠą▓č¢ą┤ą║ąŠą▓ąĖą╝ąĖ ą┤ą░ąĮąĖą╝ąĖ.










