Чисто ковалентные связи образуются между атомами одного и того же химического элемента, например, чисто ковалентной является связь хлор-хлор в молекуле Cl2. В таких молекулах распределение электронной плотности абсолютно симметрично внутри связывающей молекулярной орбитали, а максимум электронной плотности приходится на середину расстояния между ядрами. По-иному распределяется электронная плотность в ковалентных связях между атомами элементов, имеющих различную электроотрицательность.
Ядро атома более электроотрицательного элемента притягивает электрон сильнее, чем ядро атома менее электроотрицательного элемента, что может быть следствием как различия зарядов ядер атомов этих элементов, так и различия в размерах и степени заполнения электронной оболочки атомов. По этой причине распределение электронной плотности вдоль связи ассиметрично, а следовательно, атом более электроотрицательного элемента приобретает отрицательный эффективный заряд (обозначается δ-), а атом-партнер – положительный эффективный заряд (обозначается δ+). Численно эффективные заряды, реально существующие на связанных атомах, всегда меньше, чем их степени окисления.
Например, в молекуле HCl распределение электронной плотности вдоль связи H-Cl таково, что электрический «центр тяжести» отрицательного заряда смещен к атому Cl, а «центр тяжести» положительного заряда – к атому H. В результате на атомах хлора и водорода возникают эффективные заряды Hδ+-Clδ-, а связь водород-хлор приобретает частично ионный характер. В ковалентной молекуле HCl ионный характер связи составляет 17%, или полярность связи равна 17%.
Ковалентные связи между атомами, несущими некоторый эффективный заряд, называются полярными ковалентными связями. Полярность присуща большинству ковалентных связей; степень разделения зарядов вдоль связи может быть различной – от |δ| = 0 для чисто ковалентной связи до |δ| = 1 для чисто ионной связи.
Атомы, которые образуют полярную ковалентную связь, имеют признак ионов – электрический заряд. Им свойственна также другая важная характеристика ионов – относительная подвижность. Молекулы соединений с полярными связями водород-элемент часто склонны к электролитической диссоциации в растворе; такие вещества называют потенциальными электролитами.
Переход от ионной к чисто ковалентной связи можно проследить на следующих соединениях хлора с элементами третьего периода Периодической системы:
NaCl MgCl2 AlCl3 SiCl4 PCl3 SCl2 Cl2
В этом ряду соединений хлора, чисто ионная связь принадлежит соединению NaCl, а чисто ковалентная связь принадлежит соединению Cl2. Полярность связи увеличивается справа налево от Cl2 к NaCl.
Полярность ковалентной связи можно оценить по шкале электроотрицательности, предложенной и обоснованной американским химиком Полингом в 1930-х годах.
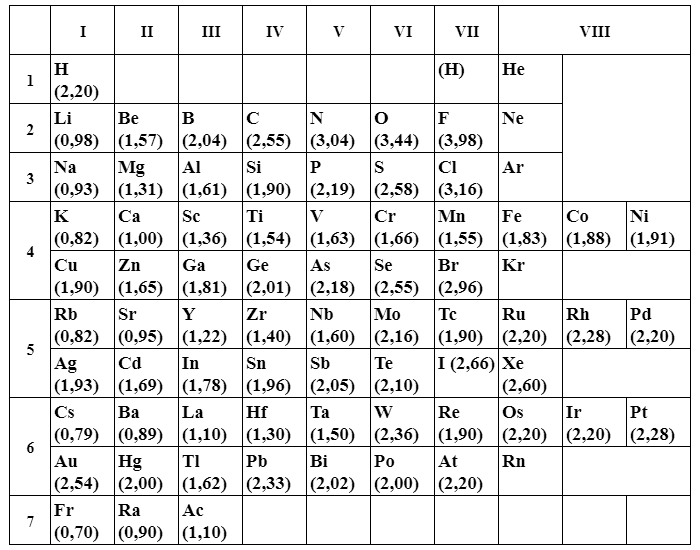
Электроотрицательность элемента (χ) – это мера притяжения электронов, которое проявляет атом данного элемента, участвующий в ковалентной связи.
Мера полярности химической связи – это разность значений электроотрицательности элементов, атомы которых образуют ковалентную связь.
|
Фтороводород HF
Вода H2O
Трифторид азота NF3
Хлороводород HCl
Аммиак NH3
Оксид хлора Cl2O
Нитрид трихлора Cl3N
Хлор Cl2
χF = 4,10
χO = 3,50
χF = 4,10
χCl = 2,83
χN = 3,07
χO = 3,50
χN = 3,07
χCl = 2,83
χH = 2,10
χH = 2,10
χN = 3,07
χH = 2,10
χH = 2,10
χCl = 2,83
χCl = 2,83
χCl = 2,83
Δχ = 2,00
Δχ = 1,40
Δχ = 1,03
Δχ = 0,73
Δχ = 0,97
Δχ = 0,67
Δχ = 0,24
Δχ = 0,00
|
Чем больше значение Δχ, тем сильнее ионный характер связи. По мере увеличения Δχ максимум электронной плотности внутри связывающей молекулярной орбитали все более сдвигаются к атомному ядру более электроотрицательного элемента. В предельном модельном случае (это чистая абстракция, т.к. не существует элемента с χ = 0) связывающие электроны полностью переходят на электронную оболочку атома более электроотрицательного элемента, и возникает чисто ионная связь.
|
Δχ
0,2
0,4
0,6
0,8
1,0
1,2
1,4
1,6
Степень ионности, %
1
4
9
15
22
30
39
47
Δχ
1,8
2,0
2,2
2,4
2,6
2,8
3,0
3,2
Степень ионности, %
55
63
70
76
82
86
89
92
|
Полинг составил шкалу, которая позволяет приближенно оценить ионности одинарных ковалентных связей по разности Δχ. По этой шкале значение Δχ = 1,7 соответствует 50% разделению зарядов, т.е. такая связь будет наполовину ковалентной, наполовину ионной.
Ниже представлена современная шкала электроотрицательности элементов по Оллерду-Рохову.
|
Элемент
Ac
Ag
Al
Am
Ar
As
At
Au
B
Ba
Be
Bi
Bk
Br
C
Ca
Cd
Ce
Cf
Cl
Cm
Co
Cr
Cs
Cu
Dy
Er
Es
Eu
F
Fe
Fm
Fr
Ga
χ
1,00
1,42
1,47
1,20
3,20
2,20
1,90
1,42
2,01
0,97
1,47
1,67
1,20
2,74
2,50
1,04
1,46
1,08
1,20
2,83
1,20
1,70
1,56
0,86
1,75
1,10
1,11
1,20
1,01
4,10
1,64
1,20
0,86
1,82
Элемент
Gd
Ge
H
He
Hf
Hg
Ho
I
In
Ir
K
Kr
La
Li
Lu
Md
Mg
Mn
Mo
N
Na
Nb
Nd
Ne
Ni
(No)
Np
O
Os
P
Pa
Pb
Pd
Pm
χ
1,11
2,02
2,10
5,50
1,23
1,44
1,10
2,21
1,49
1,55
0,91
2,94
1,08
0,97
1,14
1,20
1,23
1,60
1,30
3,07
1,01
1,23
1,07
4,84
1,75
1,20
1,22
3,50
1,52
2,10
1,14
1,55
1,35
1,07
Элемент
Po
Pr
Pt
Pu
Ra
Rb
Re
Rh
Rn
Ru
S
Sb
Sc
Se
Si
Sm
Sn
Sr
Ta
Tb
Tc
Te
Th
Ti
Tl
Tm
U
V
W
Xe
Y
Yb
Zn
Zr
χ
1,76
1,07
1,44
1,22
0,97
0,89
1,46
1,45
2,06
1,42
2,60
1,82
1,20
2,48
1,74
1,07
1,72
0,99
1,33
1,10
1,36
2,01
1,11
1,32
1,44
1,11
1,22
1,45
1,40
2,40
1,11
1,06
1,66
1,22
|
Полярные молекулы
Все двухатомные двухэлементные молекулы Aδ+-Bδ- всегда оказываются полярными, поскольку химическая связь в них ковалентная полярная. Однако многоатомные двух- и многоэлементные молекулы могут быть и полярными, и неполярными, т.к. полярность всей молекулы зависит не только от наличия в ней полярных связей, но и от геометрической формы молекул. Электрические «центры тяжести» отрицательного и положительного зарядов чаще всего не совпадают из-за различного пространственного расположения осей гибридных орбиталей центрального атома. В таких молекулах образуется электрический диполь, который представляет собой систему из разнесенных в пространстве на некоторое расстояние зарядов, небольших по числу и различных по знаку.
Полярные молекулы – это молекулы, представляющие собой электронные диполи.
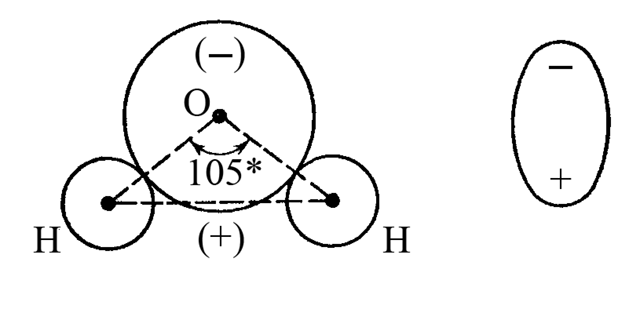
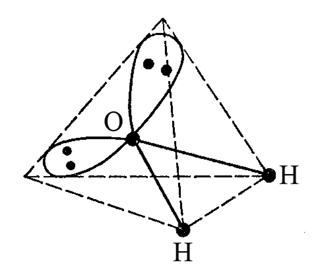
Полярной является молекула воды H2O. Каждая связь в этой молекуле полярна (Hδ+-Oδ-). Геометрия молекулы отвечает дважды незавершенному тетраэдру. Такая геометрическая форма вызывает разделение в пространстве «центров тяжести» отрицательного и положительного зарядов и образование диполя молекулы воды
Молекула аммиака NH3 также полярна
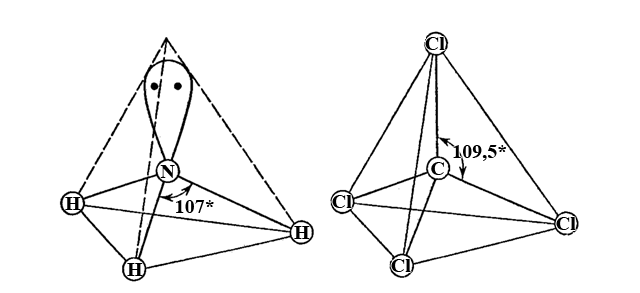
Атом N-III находится в состоянии sp3-гибридизации и в одну из вершин направлена неподеленная пара электронов атома азота (незавершенный тетраэдр). В отличие от молекулы аммиака молекула тетрахлорида углерода CCl4 неполярна; атом C+IV также имеет sp3-гибридизацию орбиталей, что отвечает геометрии правильного тетраэдра (валентный угол 109,5*). Однако и в молекуле NH3, и в молекуле CCl4 каждая связь (N-H, C-Cl) полярна.










