
ą®ąŠ čéą░ą║ąĄ ą┐ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé? ą»ą║ ą┐čĆą░čåčÄčö ą┐ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé? ąÜąŠčĆąŠčéą║ąĖą╣ ąŠą│ą╗čÅą┤ č¢čüč鹊čĆč¢čŚ – ą▓ąĖąĮąĖą║ąĮąĄąĮąĮčÅ č¢ čĆąŠąĘą▓ąĖč鹊ą║ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓. ąĪčāčćą░čüąĮč¢ ą┐ą░ą╗ąĖą▓ąĮč¢ ąĄą╗ąĄą╝ąĄąĮčéąĖ – čéąĖą┐ąĖ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓. ą¤ąĄčĆąĄą▓ą░ą│ąĖ čéą░ ąĮąĄą┤ąŠą╗č¢ą║ąĖ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓.
ąÆ 1839 čĆąŠčåč¢ ą▓ čüč¢čćąĮąĄą▓ąŠą╝čā ąĮąŠą╝ąĄčĆč¢ ŌĆ£ążč¢ą╗ąŠčüąŠčäčüčīą║ąŠą│ąŠ ąČčāčĆąĮą░ą╗čāŌĆØ ąŻč¢ą╗čīčÅą╝ ąĀąŠą▒ąĄčĆčé ąōčĆąŠą▓ (1811-1896) čĆąŠąĘą╝č¢čüčéąĖą▓ ąŠą┐ąĖčü ą┐ąŠą▒č¢čćąĮąŠą│ąŠ ąĄč乥ą║čéčā ą┤ąŠ ą┤ąŠčüą╗č¢ą┤čā ąĘ čĆąŠąĘą║ą╗ą░ą┤ą░ąĮąĮčÅ ą▓ąŠą┤ąĖ ąĄą╗ąĄą║čéčĆąĖčćąĮąĖą╝ čüčéčĆčāą╝ąŠą╝: ŌĆ£ąĪčéčĆč¢ą╗ą║ą░ ą│ą░ą╗čīą▓ą░ąĮąŠą╝ąĄčéčĆčā ą▓č¢ą┤čģąĖą╗čÅčöčéčīčüčÅ, ą║ąŠą╗ąĖ ą╣ąŠą│ąŠ ąĘŌĆÖčöą┤ąĮčāčÄčéčī ąĘ ą┤ą▓ąŠą╝ą░ ą┐ą╗ą░čéąĖąĮąŠą▓ąĖą╝ąĖ ąĄą╗ąĄą║čéčĆąŠą┤ą░ą╝ąĖ, čēąŠ ąĘą░ąĮčāčĆąĄąĮč¢ ą▓ čĆąŠąĘčćąĖąĮ ąĘ čĆąŠąĘą▒ą░ą▓ą╗ąĄąĮąŠčÄ čüčāą╗čīčäą░čéąĮąŠčÄ ą║ąĖčüą╗ąŠč鹊čÄ; ąŠą┤ąĖąĮ ąĘ ąĄą╗ąĄą║čéčĆąŠą┤č¢ą▓ ąŠą▒ą┤čāą▓ą░čÄčéčī ą▓ąŠą┤ąĮąĄą╝, ą░ č¢ąĮčłąĖą╣ – ą║ąĖčüąĮąĄą╝.ŌĆØ – čéą░ą║ ą▒čāą╗ąŠ čüčéą▓ąŠčĆąĄąĮąŠ ą┐ąĄčĆčłąĖą╣ ą┐ą░ą╗ąĖą▓ąĮąĖą╣, ą▓ąŠą┤ąĮąĄą▓ąŠ-ą║ąĖčüąĮąĄą▓ąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé.
ąŚą│ą░ą┤ą░ą╣č鹥 ą┤ąŠčüą╗č¢ą┤, ą▓ ą┐čĆąŠą▒č¢čĆą║čā ąĮą░ą╗ąĖą▓ą░čÄčéčī čĆąŠąĘčćąĖąĮ čģą╗ąŠčĆąĖą┤ąĮąŠčŚ ą║ąĖčüą╗ąŠčéąĖ, ą┤ąŠą┤ą░čÄčéčī čłą╝ą░č鹊č湊ą║ čåąĖąĮą║čā č¢ ąĘą░ą║čĆąĖą▓ą░čÄčéčī ą┐čĆąŠą▒ą║ąŠčÄ ąĘč¢ čüą║ą╗čÅąĮąŠčÄ čéčĆčāą▒ą║ąŠčÄ ąĘ č鹊ąĮą║ąĖą╝ ą║č¢ąĮčåąĄą╝. ąÆąŠą┤ąĄąĮčī, čēąŠ ą▓ąĖą┤č¢ą╗čÅčöčéčīčüčÅ ą┐č¢ą┤ą┐ą░ą╗čÄčÄčéčī. ąĪą┐ąŠčüč鹥čĆč¢ą│ą░čÄčéčī ą│ąŠčĆč¢ąĮąĮčÅ ą▓ąŠą┤ąĮčÄ ą▓ ą║ąĖčüąĮč¢ – ą╝ą░ą╣ąČąĄ ą▒ąĄąĘą▒ą░čĆą▓ąĮąĄ, ą│ą░čĆčÅč湥 ą┐ąŠą╗čāą╝ŌĆÖčÅ.
2H2 + O2 = 2H2O; ╬öH0298 = -483,65 ą║ąöąČ
ąÉč鹊ą╝ąĖ ą│č¢ą┤čĆąŠą│ąĄąĮčā ąŠą║ąĖčüąĮčÄčÄčéčīčüčÅ: 2H2 = 4H+ + 4e–
ąÉč鹊ą╝ąĖ ąŠą║čüąĖą│ąĄąĮčā ą▓č¢ą┤ąĮąŠą▓ą╗čÄčÄčéčīčüčÅ: O2 + 4e– = 2O2-
ąÆ ą┐čĆąŠčåąĄčüč¢ ą│ąŠčĆč¢ąĮąĮčÅ ą▓ąŠą┤ąĮčÄ ą▓ ą║ąĖčüąĮč¢ ą▓č¢ą┤ą▒čāą▓ą░čöčéčīčüčÅ ąĮąĄ ą▓ą┐ąŠčĆčÅą┤ą║ąŠą▓ą░ąĮąĖą╣ čĆčāčģ ąĄą╗ąĄą║čéčĆąŠąĮč¢ą▓, ąĘ čāčéą▓ąŠčĆąĄąĮąĮčÅą╝ čģč¢ą╝č¢čćąĮąĖčģ ąĘą▓ŌĆÖčÅąĘą║č¢ą▓. ąÉč鹊ą╝ąĖ ąŠą║čüąĖą│ąĄąĮčā ą▓č¢ą┤čéčÅą│čāčÄčéčī ą┤ąŠ čüąĄą▒ąĄ ąĄą╗ąĄą║čéčĆąŠąĮąĖ ą▓č¢ą┤ ą░č鹊ą╝č¢ą▓ ą│č¢ą┤čĆąŠą│ąĄąĮčā.
ą¦ąĖ ą╝ąŠąČąĮą░ čÅą║ąŠčüčī ą▓ą┐ąŠčĆčÅą┤ą║čāą▓ą░čéąĖ čĆčāčģ ąĄą╗ąĄą║čéčĆąŠąĮč¢ą▓ ą▓ čåč¢ą╣ čģč¢ą╝č¢čćąĮč¢ą╣ čĆąĄą░ą║čåč¢čŚ, č¢ čÅą║ ąĮą░čüą╗č¢ą┤ąŠą║, ąŠčéčĆąĖą╝ą░čéąĖ ąĄą╗ąĄą║čéčĆąĖčćąĮąĖą╣ čüčéčĆčāą╝? ąÆąĖčÅą▓ąĖą╗ąŠčüčÅ – ą╝ąŠąČąĮą░.
ąÆ ą┐ą░ą╗ąĖą▓ąĮąŠą╝čā ąĄą╗ąĄą╝ąĄąĮčéč¢ ąōčĆąŠą▓ą░, ą▓ąŠą┤ąĄąĮčī ąŠą║ąĖčüąĮčÄčöčéčīčüčÅ ą║ąĖčüąĮąĄą╝, ą░ą╗ąĄ ą▓č¢ą┤ą▒čāą▓ą░čöčéčīčüčÅ čåąĄą╣ ą┐čĆąŠčåąĄčü čĆąŠąĘą┤č¢ą╗čīąĮąŠ, č湥čĆąĄąĘ ą┐čĆąŠą▓č¢ą┤ąĮąĖą║ ąĄą╗ąĄą║čéčĆąĖčćąĮąŠą│ąŠ čüčéčĆčāą╝čā. ąÆ čåčīąŠą╝čā ą┐čĆąŠčåąĄčüč¢ ąĮąĄą╝ą░čö ą┐ąŠą╗čāą╝ŌĆÖčÅ, čģč¢ą╝č¢čćąĮą░ čĆąĄą░ą║čåč¢čÅ ąĮč¢ą▒ąĖ čĆąŠąĘčéčÅą│čāčöčéčīčüčÅ ą▓ čćą░čüč¢ č¢ č鹥ą┐ą╗ąŠą▓ąĖą╣ ąĄč乥ą║čé ą╝ą░ą╣ąČąĄ ąĮąĄ ą┐čĆąŠčÅą▓ą╗čÅčöčéčīčüčÅ. ąÆčüčÅ ąĄąĮąĄčĆą│č¢čÅ čģč¢ą╝č¢čćąĮąŠčŚ čĆąĄą░ą║čåč¢čŚ ą┐ąĄčĆąĄčéą▓ąŠčĆčÄčöčéčīčüčÅ ą▓ ąĄąĮąĄčĆą│č¢čÄ ą▓ą┐ąŠčĆčÅą┤ą║ąŠą▓ą░ąĮąŠą│ąŠ čĆčāčģčā ąĄą╗ąĄą║čéčĆąŠąĮč¢ą▓ ą┐ąŠ ą┐čĆąŠą▓č¢ą┤ąĮąĖą║čā.
ąĀąŠą▒ąŠčéą░ ą▓ąŠą┤ąĮąĄą▓ąŠ-ą║ąĖčüąĮąĄą▓ąŠą│ąŠ ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéčā
ą»ą║ ą┐čĆą░čåčÄčö ą┐ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé?
ąÆąŠą┤ąĮąĄą╝ čéą░ ą║ąĖčüąĮąĄą╝ ąŠą▒ą┤čāą▓ą░čÄčéčī ą╝ąĄčéą░ą╗ąĄą▓č¢ ąĄą╗ąĄą║čéčĆąŠą┤ąĖ ąĘŌĆÖčöą┤ąĮą░ąĮč¢ ą┐čĆąŠą▓č¢ą┤ąĮąĖą║ąŠą╝ ąĄą╗ąĄą║čéčĆąĖčćąĮąŠą│ąŠ čüčéčĆčāą╝čā. ą¤čĆąĖ čåčīąŠą╝čā, ąĄą╗ąĄą║čéčĆąŠą┤, čÅą║ąĖą╣ ąŠą▒ą┤čāą▓ą░čöčéčīčüčÅ ą▓ąŠą┤ąĮąĄą╝, ąŠčéčĆąĖą╝čāčö ą▓č¢ą┤ ą░č鹊ą╝č¢ą▓ ą│č¢ą┤čĆąŠą│ąĄąĮčā ąĄą╗ąĄą║čéčĆąŠąĮąĖ. ąÉč鹊ą╝ąĖ ą│č¢ą┤čĆąŠą│ąĄąĮčā ą┐ąĄčĆąĄčéą▓ąŠčĆčÄčÄčéčīčüčÅ ąĮą░ ą┐čĆąŠč鹊ąĮąĖ H+. ąöą░ą╗č¢, ą┐ąŠ ą╝ąĄčéą░ą╗č¢čćąĮąŠą╝čā ą┐čĆąŠą▓č¢ą┤ąĮąĖą║čā, ąĄą╗ąĄą║čéčĆąŠąĮąĖ čĆčāčģą░čÄčéčīčüčÅ ą┤ąŠ ą┤čĆčāą│ąŠą│ąŠ ąĄą╗ąĄą║čéčĆąŠą┤čā, čÅą║ąĖą╣ ąŠą▒ą┤čāą▓ą░čöčéčīčüčÅ ą║ąĖčüąĮąĄą╝. ąŚ ą┤čĆčāą│ąŠą│ąŠ ąĄą╗ąĄą║čéčĆąŠą┤čā, ąĄą╗ąĄą║čéčĆąŠąĮąĖ ą┐ąĄčĆąĄą┤ą░čÄčéčīčüčÅ ąĮą░ ą░č鹊ą╝ąĖ ąŠą║čüąĖą│ąĄąĮčā. ąÉč鹊ą╝ąĖ ąŠą║čüąĖą│ąĄąĮčā ąĮą░ą▒čāą▓ą░čÄčéčī ąĮąĄą│ą░čéąĖą▓ąĮąŠą│ąŠ ąĘą░čĆčÅą┤čā O2-.
ą»ą║čēąŠ ą▓ čģč¢ą╝č¢čćąĮč¢ą╣ čĆąĄą░ą║čåč¢čŚ ą│ąŠčĆč¢ąĮąĮčÅ ą▓ąŠą┤ąĮčÄ ą▓ ą║ąĖčüąĮč¢, ą┐čĆąŠč鹊ąĮąĖ H+ čéą░ č¢ąŠąĮąĖ O2- ąŠą▒ŌĆÖčöą┤ąĮčāčÄčéčīčüčÅ ą╝ąŠą╗ąĄą║čāą╗čā ą▓ąŠą┤ąĖ ą▒ąĄąĘą┐ąŠčüąĄčĆąĄą┤ąĮčīąŠ
2H+ + O2- = H2O
č鹊 ą▓ ą┐ą░ą╗ąĖą▓ąĮąŠą╝čā ąĄą╗ąĄą╝ąĄąĮčéč¢ čåč¢ čćą░čüčéąĖąĮą║ąĖ čĆąŠąĘą┤č¢ą╗ąĄąĮč¢ č¢ čēąŠą▒ ąĘą▓ŌĆÖčÅąĘčāą▓ą░čéąĖ čŚčģ, ą┐ąŠčéčĆč¢ą▒ąĄąĮ ąĄą╗ąĄą║čéčĆąŠą╗č¢čé. ąÆ čÅą║ąŠčüčéč¢ ąĄą╗ąĄą║čéčĆąŠą╗č¢čéčā ą▓ąĖą║ąŠčĆąĖčüč鹊ą▓čāčÄčéčī ą▓ąŠą┤ąĮąĖą╣ čĆąŠąĘčćąĖąĮ ą║ą░ą╗č¢ą╣ ą│č¢ą┤čĆąŠą║čüąĖą┤čā, čÅą║ąĖą╣ ą╝č¢čüčéąĖčéčī č¢ąŠąĮąĖ OH– č¢ K+.
ąóą░ą║ąĖą╝ čćąĖąĮąŠą╝ ą╝ą░čöą╝ąŠ čüąĖčüč鹥ą╝čā čüą║ą╗ą░ą┤ąĄąĮčā ąĘ čéčĆčīąŠčģ čäą░ąĘ:
- ą£ąĄčéą░ą╗ąĄą▓ąĖą╣ ąĄą╗ąĄą║čéčĆąŠą┤ (čéą▓ąĄčĆą┤ą░ čäą░ąĘą░);
- ąōą░ąĘąŠą┐ąŠą┤č¢ą▒ąĮč¢ ą▓ąŠą┤ąĄąĮčī čéą░ ą║ąĖčüąĄąĮčī (ą│ą░ąĘąŠą▓ą░ čäą░ąĘą░);
- ąĢą╗ąĄą║čéčĆąŠą╗č¢čé (čĆč¢ą┤ą║ą░ čäą░ąĘą░).
ąØą░ ą╝ąĄąČč¢ čåąĖčģ čéčĆčīąŠčģ čäą░ąĘ č¢ ą▓č¢ą┤ą▒čāą▓ą░čÄčéčīčüčÅ ąĄą╗ąĄą║čéčĆąŠčģč¢ą╝č¢čćąĮč¢ ą┐čĆąŠčåąĄčüąĖ ą▓ ą┐ą░ą╗ąĖą▓ąĮąŠą╝čā ąĄą╗ąĄą╝ąĄąĮčéč¢.
ąĪčģąĄą╝ą░ ą▓ąŠą┤ąĮąĄą▓ąŠ-ą║ąĖčüąĮąĄą▓ąŠą│ąŠ ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéčā (čĆąŠąĘą┤ąĖą▓č¢čéčīčüčÅ čŚčŚ čāą▓ą░ąČąĮąŠ, čēąŠą▒ ąĘčĆąŠąĘčāą╝č¢čéąĖ, čÅą║ ą┐čĆą░čåčÄčö ą┐ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé).
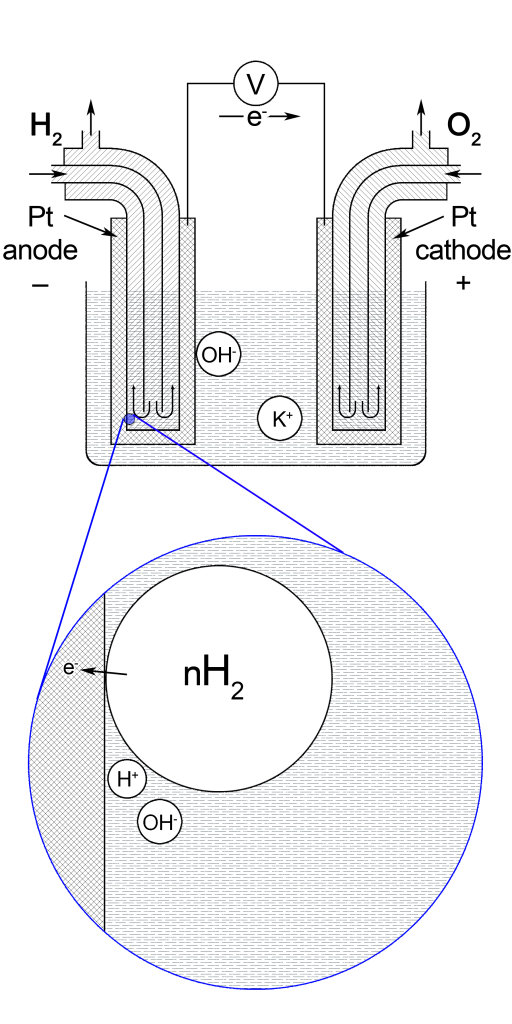
ąØą░ ą░ąĮąŠą┤č¢ ą▓ąŠą┤ąĮąĄą▓ąŠ-ą║ąĖčüąĮąĄą▓ąŠą│ąŠ ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéčā ąŠą║ąĖčüąĮčÄčöčéčīčüčÅ ą▓ąŠą┤ąĄąĮčī, ą┐čĆąŠč鹊ąĮąĖ, čÅą║č¢ čāčéą▓ąŠčĆčÄčÄčéčīčüčÅ, ąĘŌĆÖčöą┤ąĮčāčÄčéčīčüčÅ ąĘ ą│čĆčāą┐ą░ą╝ąĖ OH–:
2H2 + 4OH– = 4H2O + 4e–
ąØą░ ą║ą░č鹊ą┤č¢ ą▓ąŠą┤ąĮąĄą▓ąŠ-ą║ąĖčüąĮąĄą▓ąŠą│ąŠ ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéčā, ą▓č¢ą┤ąĮąŠą▓ą╗čÄčöčéčīčüčÅ ą║ąĖčüąĄąĮčī ą▓č¢ą┤ą┐ąŠą▓č¢ą┤ąĮąŠ ą┤ąŠ čĆąĄą░ą║čåč¢čŚ:
O2 + 4e– + 2H2O = 4OH–
ąĀąĄą░ą║čåč¢čÄ ąŠą║ąĖčüąĮąĄąĮąĮčÅ ą▓ ą┐ą░ą╗ąĖą▓ąĮąŠą╝čā ąĄą╗ąĄą╝ąĄąĮčéč¢ č¢ąĮąŠą┤č¢ ąĮą░ąĘąĖą▓ą░čÄčéčī čģąŠą╗ąŠą┤ąĮąĄ ą│ąŠčĆč¢ąĮąĮčÅ.
ąōąŠą╗ąŠą▓ąĮą░ ą┐ąĄčĆąĄą▓ą░ą│ą░ ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéčā ą┐ąĄčĆąĄą┤ ą┤ą▓ąĖą│čāąĮą░ą╝ąĖ ą▓ąĮčāčéčĆč¢čłąĮčīąŠą│ąŠ ąĘą│ąŠčĆčÅąĮąĮčÅ ą┐ąŠą╗čÅą│ą░čö ą▓ č鹊ą╝čā, čēąŠ ąĄąĮąĄčĆą│č¢čÅ čģč¢ą╝č¢čćąĮąĖčģ ą┐čĆąŠčåąĄčüč¢ą▓ ą╝ą░ą╣ąČąĄ ą┐ąŠą▓ąĮč¢čüčéčÄ ą┐ąĄčĆąĄčéą▓ąŠčĆčÄčöčéčīčüčÅ ąĮą░ ąĄą╗ąĄą║čéčĆąĖčćąĮčā ąĄąĮąĄčĆą│č¢čÄ. ąÜąŠąĄčäč¢čåč¢čöąĮčé ą║ąŠčĆąĖčüąĮąŠčŚ ą┤č¢čŚ (ąÜąÜąö) ą┤ą▓ąĖą│čāąĮą░ ą▓ąĮčāčéčĆč¢čłąĮčīąŠą│ąŠ ąĘą│ąŠčĆčÅąĮąĮčÅ, ą▓ ąĮą░ą╣č鹥čģąĮąŠą╗ąŠą│č¢čćąĮč¢čłąĖčģ ą╝ąŠą┤ąĄą╗čÅčģ ąöąÆąŚ ą╗ąĄą┤ą▓ąĄ ą┤ąŠčéčÅą│čāčö ą┤ąŠ 30%. ąÜąÜąö ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéčā 50-95%.
ą¤ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé ą╝ąŠąČąĮą░ čüčéą▓ąŠčĆąĖčéąĖ ąĮąĄ čéč¢ą╗čīą║ąĖ ąĮą░ ąŠčüąĮąŠą▓č¢ ą▓ąŠą┤ąĮčÄ č¢ ą║ąĖčüąĮčÄ. ąĪą┐ą░ą╗čÄą▓ą░čéąĖ ą╝ąŠąČąĮą░ ą▒ą░ą│ą░č鹊 čĆąĄč湊ą▓ąĖąĮ, ą┐ąĄčĆąĄčéą▓ąŠčĆčÄčÄčćąĖ ąĄąĮąĄčĆą│č¢čÄ čģč¢ą╝č¢čćąĮąŠčŚ čĆąĄą░ą║čåč¢čŚ ąĮą░ ąĄą╗ąĄą║čéčĆąĖčćąĮčā ąĄąĮąĄčĆą│č¢čÄ.
ąÆ 1897 čĆąŠčåč¢ ąÆč¢ą╗čīčÅą╝ ą¢ą░ą║ąŠ čüčéą▓ąŠčĆąĖą▓ ą┐ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé ąĘ ą┐čĆčÅą╝ąĖą╝ ąŠą║ąĖčüąĮąĄąĮąĮčÅą╝ ą▓čāą│ą╗ąĄčåčÄ. ą¤ąŠčéčāąČąĮč¢čüčéčī ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéčā ą¢ą░ą║ąŠ čüčéą░ąĮąŠą▓ąĖą╗ą░ 1,5 ą║ąÆčé. ą¤ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé ą¢ą░ą║ąŠ ą╝ą░ą▓ čéą░ą║čā ą║ąŠąĮčüčéčĆčāą║čåč¢čÄ: ąĘą░ą╗č¢ąĘąĮąĖą╣ čéą░ ą▓čāą│č¢ą╗čīąĮąĖą╣ čüčéčĆąĖąČąĮč¢ (ąĄą╗ąĄą║čéčĆąŠą┤ąĖ) ąĘą░ąĮčāčĆčÄą▓ą░ą╗ąĖ ą▓ ąĄą╗ąĄą║čéčĆąŠą╗č¢čé – čĆąŠąĘą┐ą╗ą░ą▓ą╗ąĄąĮąĖą╣ ą╗čāą│ (NaOH) č鹥ą╝ą┐ąĄčĆą░čéčāčĆąŠčÄ 400-500*ąĪ. ąŚą░ą╗č¢ąĘąĮąĖą╣ ą║ą░č鹊ą┤ ąŠą▒ą┤čāą▓ą░ą╗ąĖ ą║ąĖčüąĮąĄą╝ ą┐ąŠą▓č¢čéčĆčÅ, ą▓ čĆąĄąĘčāą╗čīčéą░čéč¢ č湊ą│ąŠ, ąĄą╗ąĄą║čéčĆąŠąĮąĖ ą▓č¢ą┤ ą▓čāą│č¢ą╗čīąĮąŠą│ąŠ ąĄą╗ąĄą║čéčĆąŠą┤čā čĆčāčģą░ą╗ąĖčüčÅ ą┤ąŠ ąĘą░ą╗č¢ąĘąĮąŠą│ąŠ ąĄą╗ąĄą║čéčĆąŠą┤čā č湥čĆąĄąĘ ą┐čĆąŠą▓č¢ą┤ąĮąĖą║. ą¤ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé ą¢ą░ą║ąŠ ą╝ą░ą▓ ąÜąÜąö 82%, čēč¢ą╗čīąĮč¢čüčéčī ąĄą╗ąĄą║čéčĆąĖčćąĮąŠą│ąŠ čüčéčĆčāą╝čā 0,1 ąÉą╝ą┐ąĄčĆ ąĘ ą║ąŠąČąĮąŠą│ąŠ ą║ą▓ą░ą┤čĆą░čéąĮąŠą│ąŠ čüą░ąĮčéąĖą╝ąĄčéčĆčā ą┐ą╗ąŠčēč¢ ąĄą╗ąĄą║čéčĆąŠą┤čā.
ąÆčāą│ą╗ąĄčåčī-ą┐ąŠą▓č¢čéčĆčÅąĮąĖą╣ ą┐ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé ą¢ą░ą║ąŠ ą▒čāą▓ ąĮą░čüčéč¢ą╗čīą║ąĖ ą▓ą┤ą░ą╗ąĖą╝, čēąŠ ą▓ č鹊ą╝čā ąČ 1897 čĆąŠčåč¢, ą¢ą░ą║ąŠ ąŠą┐čāą▒ą╗č¢ą║čāą▓ą░ą▓ ą▓ ąČčāčĆąĮą░ą╗č¢ ŌĆ£HarperŌĆÖs MagazineŌĆØ čüąĄąĮčüą░čåč¢ą╣ąĮčā čüčéą░čéčéčÄ ą┐čĆąŠ ą▓čüč¢ą╣ ą┐ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé. ąÆ čüčéą░čéčéč¢ ą¢ą░ą║ąŠ ą┤ąĄčéą░ą╗čīąĮąŠ ąŠą┐ąĖčüą░ą▓ ą┐čĆąŠąĄą║čé ąŠą║ąĄą░ąĮč¢čćąĮąŠą│ąŠ ą╗ą░ą╣ąĮąĄčĆą░ ąĘ ąĄąĮąĄčĆą│ąĄčéąĖčćąĮąŠčÄ čāčüčéą░ąĮąŠą▓ą║ąŠčÄ ąĮą░ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéą░čģ. ąóąŠą┤č¢čłąĮč¢ ą║ąŠčĆą░ą▒ą╗č¢ ą╝ą░ą╗ąĖ ą┐ą░čĆąŠą▓č¢ čéčāčĆą▒č¢ąĮąĖ, čÅą║č¢ ą┐čĆą░čåčÄą▓ą░ą╗ąĖ ąĮą░ čüą┐ą░ą╗čÄą▓ą░ąĮąĮč¢ ą▓čāą│č¢ą╗ą╗čÅ (čŚčģ ąÜąÜąö ą▒čāą▓ ą▒ą╗ąĖąĘčīą║ąŠ 10%). ą¢ą░ą║ąŠ čĆąŠąĘčĆą░čģčāą▓ą░ą▓, ąĮą░čüą║č¢ą╗čīą║ąĖ ą╝ąĄąĮčłąĄ ą┐ąŠčéčĆč¢ą▒ąĮąŠ ą▒čāą╗ąŠ ą▒ ą▓čāą│č¢ą╗ą╗čÅ, čÅą║čēąŠ ą▓ąĖą║ąŠčĆąĖčüč鹊ą▓čāą▓ą░čéąĖ ą┐ą░ą╗ąĖą▓ąĮč¢ ąĄą╗ąĄą╝ąĄąĮčéąĖ ą╣ąŠą│ąŠ ą║ąŠąĮčüčéčĆčāą║čåč¢čŚ.
ąÉą╗ąĄ ą┐ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé ą¢ą░ą║ąŠ ą╝ą░ą▓ čüčāčéčéčöą▓ąĖą╣ ąĮąĄą┤ąŠą╗č¢ą║. ąÆ ą┐čĆąŠčåąĄčüč¢ ąŠą║ąĖčüąĮąĄąĮąĮčÅ ą▓čāą│č¢ą╗čīąĮąŠą│ąŠ ąĄą╗ąĄą║čéčĆąŠą┤čā čāčéą▓ąŠčĆčÄčöčéčīčüčÅ ą║ą░čĆą▒ąŠąĮ ą┤č¢ąŠą║čüąĖą┤, čÅą║ąĖą╣ ą┐ąŠą│ą╗ąĖąĮą░čöčéčīčüčÅ ą╗čāąČąĮąĖą╝ ąĄą╗ąĄą║čéčĆąŠą╗č¢č鹊ą╝ č¢ čłą▓ąĖą┤ą║ąŠ ą╣ąŠą│ąŠ ą┐čüčāčö. ąĪčéčĆąŠą║ ąĄą║čüą┐ą╗čāą░čéą░čåč¢čŚ ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéčā ą¢ą░ą║ąŠ ą▒čāą▓ ąĘą░ąĮą░ą┤č鹊 ą╝ą░ą╗ąĖą╝.
ą¤čĆąŠčéčÅą│ąŠą╝ ą╝ą░ą╣ąČąĄ ą┐č¢ą▓ čüč鹊ą╗č¢čéčéčÅ, ą┐ąŠąŠą┤ąĖąĮąŠą║č¢ ą▓ąĖąĮą░čģč¢ą┤ąĮąĖą║ąĖ ąĮą░ą╝ą░ą│ą░ą╗ąĖčüčÅ čüčéą▓ąŠčĆčÄą▓ą░čéąĖ ąĄč乥ą║čéąĖą▓ąĮč¢ ą┐ą░ą╗ąĖą▓ąĮč¢ ąĄą╗ąĄą╝ąĄąĮčéąĖ, čÅą║č¢ ą╝ąŠąČąĮą░ ą▒ ą▒čāą╗ąŠ ą▓ąĖą║ąŠčĆąĖčüč鹊ą▓čāą▓ą░čéąĖ ą▓ ą┐čĆąŠą╝ąĖčüą╗ąŠą▓ąĖčģ ą╝ą░čüčłčéą░ą▒ą░čģ. ąÉą╗ąĄ čŚčģ čĆąŠą▒ąŠčéąĖ ąĮąĄ ą▒čāą╗ąĖ čāčüą┐č¢čłąĮąĖą╝ąĖ.
ąØą░ą┐čĆąĖą║ą╗ą░ą┤ ą▓ 1911 čĆąŠčåč¢, ą┐ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé ą¢ą░ą║ąŠ ą▒čāą╗ąŠ ą▓ą┤ąŠčüą║ąŠąĮą░ą╗ąĄąĮąŠ, ąĮąŠą▓ąĖą╣ ą┐ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé ąæą░čāčĆą░-ąĢčĆąĄąĮą▒ąĄčĆą│ą░, čéą░ą║ čüą░ą╝ąŠ ą▒čāą▓ ąĘą░čüąĮąŠą▓ą░ąĮąĖą╣ ąĮą░ ąĄą╗ąĄą║čéčĆąŠčģč¢ą╝č¢čćąĮąŠą╝čā čüą┐ą░ą╗čÄą▓ą░ąĮąĮč¢ ą▓čāą│č¢ą╗ą╗čÅ, ą▓č¢ąĮ ą╝ą░ą▓ ąÜąÜąö 90%, ą░ą╗ąĄ ą┐čĆą░ą║čéąĖčćąĮąŠą│ąŠ ąĘą░čüč鹊čüčāą▓ą░ąĮąĮčÅ ąĮąĄ ąĘąĮą░ą╣čłąŠą▓.
ąÆ 1933 čĆąŠčåč¢ ąæą░čāčĆ ą┐čāą▒ą╗č¢ą║čāčö ąŠą│ą╗čÅą┤ čĆąŠą▒č¢čé ąĘ ą▓ąĖą▓č湥ąĮąĮčÅ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓. ąå ą▓ ą┐č¢ą┤čüčāą╝ą║čā, ąæą░čāąĄčĆ ą║ąŠąĮčüčéą░čéčāčö ąĮąĄą╝ąŠąČą╗ąĖą▓č¢čüčéčī ą▓ąĖą║ąŠčĆąĖčüč鹊ą▓čāą▓ą░čéąĖ ą┐ą░ą╗ąĖą▓ąĮč¢ ąĄą╗ąĄą╝ąĄąĮčéąĖ ą▓ ą┐čĆąŠą╝ąĖčüą╗ąŠą▓ąŠčüčéč¢ čéą░ ą┐ąŠą▒čāčéč¢.
ąÉą╗ąĄ ą┐ąŠčłčāą║ąĖ ą▓ čåą░čĆąĖąĮč¢ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓ ąĮąĄ ą┐čĆąĖą┐ąĖąĮąĖą╗ąĖčüčī. ąÆ 40čģ čĆąŠą║ą░čģ ąźąź čüčé. ą×ą│ą░ąĮąĄčü ąÜą░čĆą░ą┐ąĄč鹊ą▓ąĖčć ąöą░ą▓čéčÅąĮ čüą║ąŠąĮčüčéčĆčāčÄą▓ą░ą▓ ą┐čĆąĖčüčéčĆč¢ą╣ ą┤ą╗čÅ ąĄą╗ąĄą║čéčĆąŠčģč¢ą╝č¢čćąĮąŠą│ąŠ čüą┐ą░ą╗čÄą▓ą░ąĮąĮčÅ ą│ąĄąĮąĄčĆą░č鹊čĆąĮąŠą│ąŠ ą│ą░ąĘčā (ą│ą░ąĘ čÅą║ąĖą╣ ąŠčéčĆąĖą╝čāčÄčéčī čłą╗čÅčģąŠą╝ ą│ą░ąĘąĖčäč¢ą║ą░čåč¢čŚ čéą▓ąĄčĆą┤ąŠą│ąŠ ą┐ą░ą╗ąĖą▓ą░). ą¤čĆąĖčüčéčĆč¢ą╣ ą┐čĆąĄą┤čüčéą░ą▓ą╗čÅą▓ čüąŠą▒ąŠčÄ ą║ąŠąČčāčģ, ą▓ čÅą║ąĖą╣ ą┐ąŠą┤ą░ą▓ą░ą╗ąŠčüčÅ, ąĘ ąŠą┤ąĮąŠą│ąŠ ą▒ąŠą║čā ą┐ąŠą▓č¢čéčĆčÅ, ą░ ąĘ č¢ąĮčłąŠą│ąŠ ą▒ąŠą║čā – ą│ąĄąĮąĄčĆą░č鹊čĆąĮąĖą╣ ą│ą░ąĘ. ąĪčéčĆčāą╝ąĄąĮč¢ ą│ą░ąĘč¢ą▓ ą▒čāą╗ąĖ čĆąŠąĘą┤č¢ą╗ąĄąĮč¢ čłą░čĆąŠą╝ čéą▓ąĄčĆą┤ąŠą│ąŠ ąĄą╗ąĄą║čéčĆąŠą╗č¢čéčā. ąŚ ą║ąŠąČąĮąŠą│ąŠ ą║čāą▒ąŠą╝ąĄčéčĆčā čéą░ą║ąŠą│ąŠ ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéčā ąŠčéčĆąĖą╝čāą▓ą░ą╗ąĖ ą┤ąŠ 5 ą║ąÆčé ąĄą╗ąĄą║čéčĆąĖčćąĮąŠčŚ ą┐ąŠčéčāąČąĮąŠčüčéč¢. ą”ąĄą╣ ą┐ąŠą║ą░ąĘąĮąĖą║ ą▓ 5 čĆą░ąĘč¢ą▓ ą┐ąĄčĆąĄą▓ąĖčēčāčö ąĄč乥ą║čéąĖą▓ąĮč¢čüčéčī čüčāčćą░čüąĮąŠčŚ č鹥ą┐ą╗ąŠą▓ąŠčŚ ąĄą╗ąĄą║čéčĆąŠčüčéą░ąĮčåč¢čŚ.
ą”č¢ą║ą░ą▓ąĖą╝ąĖ čö čĆąŠą▒ąŠčéąĖ ążčĆąĄąĮčüč¢čüą░ ąæąĄą║ąŠąĮą░, ą┐ąŠ čüčéą▓ąŠčĆąĄąĮąĮčÄ ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéčā. ąÆ 1939 čĆąŠčåč¢, ąæąĄą║ąŠąĮ (ąøąŠąĮą┤ąŠąĮ) čüčéą▓ąŠčĆčÄčö ą▓ąŠą┤ąĮąĄą▓ąŠ-ą║ąĖčüąĮąĄą▓ąĖą╣ ą┐ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé čÅą║ąĖą╣ ą▓ąĖą┤ą░čö 13 ą╝č¢ą╗č¢ą░ą╝ą┐ąĄčĆ ąĘ ą║ą▓ą░ą┤čĆą░čéąĮąŠą│ąŠ čüą░ąĮčéąĖą╝ąĄčéčĆčā ąĘąŠą▓ąĮč¢čłąĮčīąŠčŚ ąĄą╗ąĄą║čéčĆąŠą┤ąĮąŠčŚ ą┐ą╗ąŠčēč¢, ą┐čĆą░čåčÄčö ą┐čĆąĖ 100*ąĪ č¢ ą┐č¢ą┤ čéąĖčüą║ąŠą╝ 200 ą░čéą╝ąŠčüč乥čĆ. ą”ąĄą╣ ą┐ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé ą┐čĆąŠą┐čĆą░čåčÄą▓ą░ą▓ ą╗ąĖčłąĄ 48 ą│ąŠą┤ąĖąĮ.
ąæąĄą║ąŠąĮ ą┐čĆą░čåčÄą▓ą░ą▓ 10 čĆąŠą║č¢ą▓ č¢ ą┤ąŠ 1950 čĆąŠą║čā čüčéą▓ąŠčĆąĖą▓ ą┐ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé, čÅą║ąĖą╣ ą┐čĆą░čåčÄčö ą┐čĆąĖ 200*ąĪ, ą┐č¢ą┤ čéąĖčüą║ąŠą╝ 27 ą░čéą╝ąŠčüč乥čĆ č¢ ą▓ąĖą┤ą░čö 230 ą╝č¢ą╗č¢ą░ą╝ą┐ąĄčĆ ąĮą░ ą║ą▓ą░ą┤čĆą░čéąĮąĖą╣ čüą░ąĮčéąĖą╝ąĄčéčĆ ąĘąŠą▓ąĮč¢čłąĮčīąŠčŚ ąĄą╗ąĄą║čéčĆąŠą┤ąĮąŠčŚ ą┐ą╗ąŠčēč¢. ą”ąĄą╣ ąĘčĆą░ąĘąŠą║ ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéčā ą╝č¢ą│ ą┐čĆą░čåčÄą▓ą░čéąĖ čéąĖčüčÅčćč¢ ą│ąŠą┤ąĖąĮ.
ą®ąĄ č湥čĆąĄąĘ 10 čĆąŠą║č¢ą▓, ą▓ 1969 čĆąŠčåč¢, ążčĆąĄąĮčüč¢čü ąæąĄą║ąŠąĮ čüą║ąŠąĮčüčéčĆčāčÄą▓ą░ą▓ ą▒ą░čéą░čĆąĄčÄ ąĘ 40 ą║ąŠą╝č¢čĆąŠą║ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓, ąĘą░ą│ą░ą╗čīąĮąŠčÄ ą┐ąŠčéčāąČąĮč¢čüčéčÄ 6 ą║ąÆčé č¢ ąÜąÜąö 80%. ąĀąŠąĘą╝č¢čĆąĖ ą▒ą░čéą░čĆąĄčŚ ąæąĄą║ąŠąĮą░ 76 čģ 38 čģ 30 čüą╝. ą”č¢čöčŚ ą┐ąŠčéčāąČąĮąŠčüčéč¢ ą▓ąČąĄ ą▓ąĖčüčéą░čćą░ą╗ąŠ, čēąŠą▒ ą┐čĆąĖą▓ąĄčüčéąĖ ą┤ąŠ čĆčāčģčā ąĄą╗ąĄą║čéčĆąŠą╝ąŠą▒č¢ą╗čī. ąÉą╗ąĄ ą╝ą░čüą░ ą┐čĆąĖčüčéčĆąŠčÄ, čĆą░ąĘąŠą╝ ąĘ ą▒ą░ą╗ąŠąĮą░ą╝ąĖ ą▒čāą╗ą░ ąĘą░ąĮą░ą┤č鹊 ą▓ąĖčüąŠą║ąŠčÄ, ą▒ą╗ąĖąĘčīą║ąŠ 300 ą║č¢ą╗ąŠą│čĆą░ą╝č¢ą▓.
ąæčāą╗ąĖ č¢ č¢ąĮčłč¢ ąĮąĄą┤ąŠą╗č¢ą║ąĖ ą▓ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéą░čģ 50-70-čģ čĆąŠą║č¢ą▓ ąźąź čüčé. ąÜčĆč¢ą╝ ą╝ą░čüąĖ ą║ąŠąĮčüčéčĆčāą║čåč¢čŚ, ąĄč乥ą║čéąĖą▓ąĮč¢ ą┐ą░ą╗ąĖą▓ąĮč¢ ąĄą╗ąĄą╝ąĄąĮčéąĖ ą┐čĆą░čåčÄą▓ą░ą╗ąĖ ąĮą░ ąŠčćąĖčēąĄąĮąŠą╝čā ą▓ąŠą┤ąĮč¢, čÅą║ąĖą╣ ą║ąŠčłčéčāą▓ą░ą▓ ą▓ čéč¢ čćą░čüąĖ ąĘą░ąĮą░ą┤č鹊 ą┤ąŠčĆąŠą│ąŠ. ąÜą░čéą░ą╗č¢ąĘą░č鹊čĆąĖ, čÅą║č¢ ą▓ąĖą║ąŠčĆąĖčüč鹊ą▓čāą▓ą░ą╗ąĖ ą▓ ą┐ą░ą╗ąĖą▓ąĮąŠą╝čā ąĄą╗ąĄą╝ąĄąĮčéč¢, ąĮą░ ąĄą╗ąĄą║čéčĆąŠą┤ą░čģ, ą┤čāąČąĄ čćčāčéą╗ąĖą▓č¢ ą┤ąŠ ąĘą░ą▒čĆčāą┤ąĮąĄąĮčī, č¢ čłą▓ąĖą┤ą║ąŠ ą┐čüčāčÄčéčīčüčÅ.
ąØą░čüčéčāą┐ąĮąĖą╣ ąĄčéą░ą┐ čĆąŠąĘą▓ąĖčéą║čā ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓ čüčāą┐čĆąŠą▓ąŠą┤ąČčāą▓ą░ą▓ ą░ąĄčĆąŠą║ąŠčüą╝č¢čćąĮčā čüč乥čĆčā.
ąÜąŠą╗ąĖ ą▓ąĖčĆč¢čłčāą▓ą░ą╗ąĖ ą┐ąĖčéą░ąĮąĮčÅ ąĄąĮąĄčĆą│ąĄčéąĖčćąĮąŠčŚ čāčüčéą░ąĮąŠą▓ą║ąĖ ą┤ą╗čÅ ąČąĖą▓ą╗ąĄąĮąĮčÅ ą║ąŠčüą╝č¢čćąĮąĖčģ ą░ą┐ą░čĆą░čéč¢ą▓, ą┐čĆąŠą▓ąĄą╗ąĖ ą┐ąŠčĆč¢ą▓ąĮčÅąĮąĮčÅ. ą®ąŠą▒ ąĘą░ą┤ąŠą▓ąŠą╗čīąĮąĖčéąĖ ą┐ąŠčéčĆąĄą▒ąĖ ą▓ ąĄą╗ąĄą║čéčĆąŠąĄąĮąĄčĆą│č¢čŚ ą║ąŠčüą╝č¢čćąĮąŠą│ąŠ ą░ą┐ą░čĆą░čéčā ą┐čĆąŠčéčÅą│ąŠą╝ ą┤ą▓ąŠčģ čéąĖąČąĮč¢ą▓, ąĮąĄąŠą▒čģč¢ą┤ąĮą░ ą┐ąŠčéčāąČąĮč¢čüčéčī 200 ą║ąÆčé-ą│ąŠą┤ ąĄą╗ąĄą║čéčĆąŠąĄąĮąĄčĆą│č¢čŚ (1 ą║ąÆčé-ą│ąŠą┤ąĖąĮą░ – čåąĄ čĆąŠą▒ąŠčéą░ ą┐čĆąĖčüčéčĆąŠčÄ ą┐ąŠčéčāąČąĮč¢čüčéčÄ 1 ą║ąÆčé ą┐čĆąŠčéčÅą│ąŠą╝ ą│ąŠą┤ąĖąĮąĖ; 1 ąÆčé = 1 ąöąČ/čüąĄą║čāąĮą┤čā ąĄąĮąĄčĆą│č¢čŚ, ąŠčéąČąĄ 1 ą║ąÆčé = 1 ą║ąöąČ/čüąĄą║čāąĮą┤čā, ą┐čĆąŠčéčÅą│ąŠą╝ ą│ąŠą┤ąĖąĮąĖ čéą░ą║ąĖą╣ ą┐čĆąĖčüčéčĆč¢ą╣ čüą┐ąŠąČąĖą▓ą░čö 3600 ą║ąöąČ ąĄąĮąĄčĆą│č¢čŚ). ąóą░ą║čā ą┐ąŠčéčāąČąĮč¢čüčéčī ąĘą░ą┤ąŠą▓ąŠą╗čīąĮčÅčö čüčāčćą░čüąĮąĖą╣ čüčĆč¢ą▒ąĮąŠ-čåąĖąĮą║ąŠą▓ąĖą╣ ą░ą║čāą╝čāą╗čÅč鹊čĆ ą╝ą░čüąŠčÄ 1.5 č鹊ąĮąĮąĖ, čÅą║ąĖą╣ ąĘą░ą╣ą╝ą░čö ąŠą▒ŌĆÖčöą╝ 0,5 ą╝3, ą┤ąŠ ą░ą║čāą╝čāą╗čÅč鹊čĆčā, čēąŠą▒ ą╣ąŠą│ąŠ ąĘą░čĆčÅą┤ąČą░čéąĖ, ą┐ąŠčéčĆč¢ą▒ąĮč¢ čüąŠąĮčÅčćąĮč¢ ą┐ą░ąĮąĄą╗č¢, ą╝ą░čüąŠčÄ 335 ą║č¢ą╗ąŠą│čĆą░ą╝ č¢ ąŠą▒ŌĆÖčöą╝ąŠą╝ 1,12 ą╝3. ąŚą░ą│ą░ą╗čīąĮą░ ą╝ą░čüą░ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓ ąČąĖą▓ą╗ąĄąĮąĮčÅ ą║ąŠčüą╝č¢čćąĮąŠą│ąŠ ą░ą┐ą░čĆą░čéčā 1835 ą║ą│ č¢ ąŠą▒ŌĆÖčöą╝ 1,62 ą╝3.
ąĢąĮąĄčĆą│ąŠčāčüčéą░ąĮąŠą▓ą║ą░ čéą░ą║ąŠčŚ čüą░ą╝ąŠčŚ ą┐ąŠčéčāąČąĮąŠčüčéč¢ ąĮą░ ą▓ąŠą┤ąĮąĄą▓ąŠ-ą║ąĖčüąĮąĄą▓ąĖčģ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéą░čģ ą╝ą░čö ą╝ą░čüčā 225 ą║ą│ č¢ ąĘą░ą╣ą╝ą░čö ąŠą▒ŌĆÖčöą╝ 0,45 ą╝3. ąĀč¢ąĘąĮąĖčåčÅ ąĮą░ąŠčćąĮą░.
ąÜčĆč¢ą╝ ą║ąŠą╝ą┐ą░ą║čéąĮąĖčģ čĆąŠąĘą╝č¢čĆč¢ą▓, ą▓ąŠą┤ąĮąĄą▓ąŠ-ą║ąĖčüąĮąĄą▓č¢ ą┐ą░ą╗ąĖą▓ąĮč¢ ąĄą╗ąĄą╝ąĄąĮčéąĖ ą╝ą░čÄčéčī č¢ č¢ąĮčłč¢ ą┐ąĄčĆąĄą▓ą░ą│ąĖ. ą¤ą░ą╗ąĖą▓ąĮč¢ ąĄą╗ąĄą╝ąĄąĮčéąĖ ą│ąĄąĮąĄčĆčāčÄčéčī ąĄą╗ąĄą║čéčĆąĖčćąĮčā ąĄąĮąĄčĆą│č¢čÄ ąĮąĄąĘą░ą╗ąĄąČąĮąŠ ą▓č¢ą┤ ąŠčüą▓č¢čéą╗ąĄąĮąŠčüčéč¢ (čüąŠąĮčÅčćąĮč¢ ą▒ą░čéą░čĆąĄčŚ – ą╗ąĖčłąĄ ą┐č¢ą┤ ą▓ą┐ą╗ąĖą▓ąŠą╝ čüą▓č¢čéą╗ą░). ą¤ą░ą╗ąĖą▓ąĮč¢ ąĄą╗ąĄą╝ąĄąĮčéąĖ ą╝ąŠąČčāčéčī ą╝ą░čéąĖ ą▒čāą┤čī-čÅą║čā ą│ąĄąŠą╝ąĄčéčĆąĖčćąĮčā č乊čĆą╝čā; ą▓ąŠąĮąĖ ąĮąĄ čćčāčéą╗ąĖą▓č¢ ą┤ąŠ čāą┤ą░čĆč¢ą▓, ą▓č¢ą▒čĆą░čåč¢ą╣ čĆą░ą┤č¢ą░čåč¢čŚ, ą▓ąĖčéčĆąĖą╝čāčÄčéčī ą║ąŠčĆąŠčéą║ąŠčćą░čüąĮč¢ ą┐ąĄčĆąĄą▓ą░ąĮčéą░ąČąĄąĮąĮčÅ ą┤ąŠ 100% ą▓č¢ą┤ ąĮąŠą╝č¢ąĮą░ą╗čīąĮąŠčŚ ą┐ąŠčéčāąČąĮąŠčüčéč¢. ą¤ą░ą╗ąĖą▓ąĮč¢ ąĄą╗ąĄą╝ąĄąĮčéąĖ ąĮąĄ ą╝ą░čÄčéčī čłą║č¢ą┤ą╗ąĖą▓ąĖčģ ą▓ąĖą║ąĖą┤č¢ą▓ č¢ ąĮąĄą▒ąĄąĘą┐ąĄčćąĮąĖčģ ą║ąŠą╝ą┐ąŠąĮąĄąĮčéč¢ą▓ (ąĮą░ ą▓č¢ą┤ą╝č¢ąĮčā ą▓č¢ą┤ čüčĆč¢ą▒ąĮąŠ-čåąĖąĮą║ąŠą▓ąŠą│ąŠ ą░ą║čāą╝čāą╗čÅč鹊čĆčā), ą▓ąŠąĮąĖ ą▒ąĄąĘčłčāą╝ąĮč¢, ąĮąĄ čüčéą▓ąŠčĆčÄčÄčéčī čĆą░ą┤č¢ąŠą┐ąĄčĆąĄčłą║ąŠą┤ č¢ čłą║č¢ą┤ą╗ąĖą▓ąĖčģ ą▓ąĖą┐čĆąŠą╝č¢ąĮčÄą▓ą░ąĮčī, ą┐čĆą░čåčÄčÄčéčī ą┐čĆąĖ č鹥ą╝ą┐ąĄčĆą░čéčāčĆą░čģ ą▒ą╗ąĖąĘčīą║ąĖčģ ą┤ąŠ 20*ąĪ.
ąÆ čüąĄčĆąĄą┤ąĖąĮč¢ 60-čģ čĆąŠą║č¢ą▓ ąźąź čüčé. ąĮą░ą┤ čüčéą▓ąŠčĆąĄąĮąĮčÅą╝ ąĄč乥ą║čéąĖą▓ąĮąĖčģ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓ (č¢ąĮčłą░ ąĮą░ąĘą▓ą░ ą┐čĆąĖčéą░ą╝ą░ąĮąĮą░ čåčīąŠą╝čā ą┐ąĄčĆč¢ąŠą┤čā ąĄą╗ąĄą║čéčĆąŠčģč¢ą╝č¢čćąĮąĖą╣ ą│ąĄąĮąĄčĆą░č鹊čĆ) ą┐čĆą░čåčÄą▓ą░čéąĖ ą┤ąĄčüčÅčéą║ąĖ čéąĖčüčÅčć ąĮą░čāą║ąŠą▓čåč¢ą▓ ą┐ąŠ ą▓čüčīąŠą╝čā čüą▓č¢čéčā. ąŻčĆčÅą┤ąĖ ą▓ąĖčéčĆą░čćą░ą╗ąĖ ąĮą░ ąŠą┐ą╗ą░čéčā ąĮą░čāą║ąŠą▓ąŠ-č鹥čģąĮč¢čćąĮąŠčŚ čĆąŠą▒ąŠčéąĖ ą┐ąŠ čüčéą▓ąŠčĆąĄąĮąĮčÄ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓ čüąŠčéąĮč¢ ą╝č¢ą╗čīą╣ąŠąĮč¢ą▓ ą┤ąŠą╗ą░čĆč¢ą▓ čēąŠčĆąŠą║čā.
ąÆ ą▓ąĖą║ąŠčĆąĖčüčéą░ąĮąĮč¢ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓ ą▓ ą║ąŠčüą╝č¢čćąĮč¢ą╣ čüč乥čĆč¢ čö ąĮąĄą┤ąŠą╗č¢ą║. ą¤ą░ą╗ąĖą▓ąŠ čéčĆąĄą▒ą░ ą┤ąŠčüčéą░ą▓ą╗čÅčéąĖ ą▓ ą║ąŠčüą╝ąŠčü. ąØąĄčüą║ą╗ą░ą┤ąĮč¢ čĆąŠąĘčĆą░čģčāąĮą║ąĖ ą┐ąŠą║ą░ąĘčāčÄčéčī, čēąŠ ą┤ą╗čÅ ąĘą░ą▒ąĄąĘą┐ąĄč湥ąĮąĮčÅ ą┐ąŠčéčāąČąĮąŠčüčéč¢ 200 ą║ąÆčé*ą│ąŠą┤ ą┐čĆąŠčéčÅą│ąŠą╝ ą┤ą▓ąŠčģ čéąĖąČąĮč¢ą▓, ą┤ą╗čÅ ą║ąŠčüą╝č¢čćąĮąŠą│ąŠ ą░ą┐ą░čĆą░čéčā, ąĮąĄąŠą▒čģč¢ą┤ąĮąŠ 100 ą║ą│ ą▓ąŠą┤ąĮčÄ č¢ ą║ąĖčüąĮčÄ. ąÜčĆč¢ą╝ čåčīąŠą│ąŠ, č¢ąĮąČąĄąĮąĄčĆąĖ-čĆąŠąĘčĆąŠą▒ąĮąĖą║ąĖ ąĘč¢čłč鹊ą▓čģąĮčāą╗ąĖčüčÅ ąĘ ą▒ą░ą│ą░čéčīą╝ą░ č鹥čģąĮąŠą╗ąŠą│č¢čćąĮąĖą╝ąĖ čüą║ą╗ą░ą┤ąĮąŠčēą░ą╝ąĖ ą▓ąĖą║ąŠčĆąĖčüčéą░ąĮąĮčÅ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓ ą▓ ą║ąŠčüą╝ąŠčüč¢ – čéą░ą║ ąĘą▓ą░ąĮč¢ T, P, g-ąĮčāą╗č¢ (ąĮčāą╗čīąŠą▓č¢ č鹥ą╝ą┐ąĄčĆą░čéčāčĆą░, čéąĖčüą║, ą│čĆą░ą▓č¢čéą░čåč¢čÅ).
ąØąĄąĘą▓ą░ąČą░čÄčćąĖ ąĮą░ č鹥čģąĮąŠą╗ąŠą│č¢čćąĮč¢ čüą║ą╗ą░ą┤ąĮąŠčēč¢, ą▓ 1968 čĆąŠčåč¢, ą▓ą┤ąŠčüą║ąŠąĮą░ą╗ąĄąĮč¢ ą┐ą░ą╗ąĖą▓ąĮč¢ ąĄą╗ąĄą╝ąĄąĮčéąĖ ąæąĄą║ąŠąĮą░ ąĘą░ą▒ąĄąĘą┐ąĄčćčāą▓ą░ą╗ąĖ čĆąŠą▒ąŠčéčā ąĄą╗ąĄą║čéčĆąŠąĮąĮąĖčģ ą║ąŠą╝ą┐ąŠąĮąĄąĮčéč¢ą▓ ą║ąŠčüą╝č¢čćąĮąĖčģ ą░ą┐ą░čĆą░čéč¢ą▓ ŌĆ£ąÉą┐ąŠą╗ą╗ąŠąĮŌĆØ č¢ ą┐ąŠą▒čāą▓ą░ą╗ąĖ ąĮą░ ą╝č¢čüčÅčåč¢. ąÆąŠą┤ąĮąĄą▓ąŠ-ą║ąĖčüąĮąĄą▓č¢ ą┐ą░ą╗ąĖą▓ąĮč¢ ąĄą╗ąĄą╝ąĄąĮčéąĖ čö ą┤ąČąĄčĆąĄą╗ąŠą╝ ą┐ąĖčéąĮąŠčŚ ą▓ąŠą┤ąĖ ą┤ą╗čÅ ą║ąŠčüą╝ąŠąĮą░ą▓čéč¢ą▓ ą▓ ą┐čĆąŠčåąĄčüč¢ ą║ąŠčüą╝č¢čćąĮąŠčŚ ą┐ąŠą┤ąŠčĆąŠąČč¢.
ąĢč乥ą║čéąĖą▓ąĮč¢čüčéčī ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓ ą▓ ą┐čĆąŠą│čĆą░ą╝č¢ ŌĆ£ąÉą┐ąŠą╗ąŠąĮŌĆØ čüčéą░ąĮąŠą▓ąĖą╗ą░ 40,4 ą║ą│/ą║ąÆčé. ąÆ ą┐čĆąŠčåąĄčüč¢ ą┐č¢ą┤ą│ąŠč鹊ą▓ą║ąĖ čéą░ ąĘą░ čĆąĄąĘčāą╗čīčéą░čéą░ą╝ąĖ ą║ąŠčüą╝č¢čćąĮąŠčŚ ąĄą║čüą┐ąĄą┤ąĖčåč¢čŚ, ą▒čāą╗ąĖ ą▓ąĖčÅą▓ą╗ąĄąĮč¢ čéą░ čāčüčāąĮčāčéč¢ čüčāčéčéčöą▓č¢ č鹥čģąĮč¢čćąĮč¢ ąĮąĄą┤ąŠą╗č¢ą║ąĖ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓ ąæąĄą║ąŠąĮą░.
ąÆ ąĮąŠą▓ąŠą╝čā ą║ąŠčüą╝č¢čćąĮąŠą╝čā ą┐čĆąŠąĄą║čéč¢ ŌĆ£OrbiterŌĆØ ą▓ąĖą║ąŠčĆąĖčüč鹊ą▓čāą▓ą░ą╗ąĖ ą▓ą┤ąŠčüą║ąŠąĮą░ą╗ąĄąĮč¢ ą┐ą░ą╗ąĖą▓ąĮč¢ ąĄą╗ąĄą╝ąĄąĮčéąĖ, ąĘ ą║ą░ą┐č¢ą╗čÅčĆąĮąĖą╝ąĖ ą╝ąĄą╝ą▒čĆą░ąĮą░ą╝ąĖ (ą┤čĆč¢ą▒ąĮąŠą┐ąŠčĆąĖčüčéąĖą╣ ą░čüą▒ąĄčüčé), č¢ ą▒ą░ą│ą░čéčīą╝ą░ č¢ąĮčłąĖą╝ąĖ čāą┤ąŠčüą║ąŠąĮą░ą╗ąĄąĮąĮčÅą╝ąĖ, ąĘą░ą▓ą┤čÅą║ąĖ čÅą║ąĖą╝ ąĄč乥ą║čéąĖą▓ąĮč¢čüčéčī ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓ ą▓ ą┐čĆąŠąĄą║čéč¢ ŌĆ£OrbiterŌĆØ ą▒čāą╗ą░ 3,63 ą║ą│/ą║ąÆčé!
ąŻ 80-čģ čĆąŠą║ą░čģ ąźąź čüčé. ą▒čāą╗ą░ ą┤ąŠčüčÅą│ąĮčāčéą░ ąĄč乥ą║čéąĖą▓ąĮč¢čüčéčī ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓ ąĮą░ čĆč¢ą▓ąĮč¢ 1,80 ą║ą│/ą║ąÆčé.
ąĪąĖą╗ą░ čüčéčĆčāą╝čā ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓
ą×ą┤ąĮč¢čöčÄ ąĘ čģą░čĆą░ą║č鹥čĆąĖčüčéąĖą║ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓ čö čüąĖą╗ą░ čüčéčĆčāą╝čā, čÅą║čā ą┐ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé ąĘą┤ą░čéąĮąĖą╣ ą│ąĄąĮąĄčĆčāą▓ą░čéąĖ. ą¤ąĄčĆčłąĖą╣ ą┐ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé ąæąĄą║ąŠąĮą░ ą╝ą░ą▓ čüąĖą╗čā čüčéčĆčāą╝čā 13 ą╝č¢ą╗č¢ą░ą╝ą┐ąĄčĆ ąĘ 1 čüą╝2 ąĘąŠą▓ąĮč¢čłąĮčīąŠčŚ ą┐ąŠą▓ąĄčĆčģąĮč¢ ąĄą╗ąĄą║čéčĆąŠą┤čā.
ąĪąĖą╗ą░ čüčéčĆčāą╝čā ą▓ąĖą╝č¢čĆčÄčöčéčīčüčÅ ą▓ ąÉą╝ą┐ąĄčĆą░čģ. 1 ąÉą╝ą┐ąĄčĆ čåąĄ čłą▓ąĖą┤ą║č¢čüčéčī čĆčāčģčā ąĘą░čĆčÅą┤čā 1 ą║čāą╗ąŠąĮ/čüąĄą║čāąĮą┤čā. 1 ą╝ąŠą╗čī ąĄą╗ąĄą║čéčĆąŠąĮč¢ą▓ ą╝ą░čö ąĘą░čĆčÅą┤ 96484,56 ą║čāą╗ąŠąĮ.
ąØą░ą┐čĆąĖą║ą╗ą░ą┤, čēąŠą▒ ą┐čĆąĖ ąĄą╗ąĄą║čéčĆąŠą╗č¢ąĘč¢ čĆąŠąĘčćąĖąĮčā ą░čĆą│ąĄąĮčéčāą╝ ąĮč¢čéčĆą░čéčā (AgNO3) ą┐čĆąŠčéčÅą│ąŠą╝ ą│ąŠą┤ąĖąĮąĖ, ąĮą░ ąĄą╗ąĄą║čéčĆąŠą┤č¢ ą▓č¢ą┤ąĮąŠą▓ąĖą╗ą░čüčÅ ą╝ą░čüą░ čüčĆč¢ą▒ą╗ą░ ą▓ 4,0247 ą│čĆą░ą╝ąĖ, ąĮąĄąŠą▒čģč¢ą┤ąĮąŠ ą┤ąŠą║ą╗ą░čüčéąĖ čüčéčĆčāą╝ čüąĖą╗ąŠčÄ ą▓ 1 ąÉą╝ą┐ąĄčĆ (ą┤ąĖą▓č¢čéčīčüčÅ ąĘą░ą║ąŠąĮąĖ ążą░čĆą░ą┤ąĄčÅ).
ą»ą║čēąŠ ą┐ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé ą│ąĄąĮąĄčĆčāčö čüąĖą╗čā čüčéčĆčāą╝čā 13 ą╝č¢ą╗č¢ą░ą╝ą┐ąĄčĆ, ą░ą▒ąŠ 0,013 ąÉ ąĘ 1 čüą╝2, č鹊 čåąĄ ąŠąĘąĮą░čćą░čö, čēąŠ ąĘą░ 1 čüąĄą║čāąĮą┤čā č湥čĆąĄąĘ ą┐ą╗ąŠčēčā 1 čüą╝2 ą┐čĆąŠčģąŠą┤ąĖčéčī 0,013 ą║čāą╗ąŠąĮ ąĘą░čĆčÅą┤čā, ą░ą▒ąŠ 0,013 ąÜą╗ / 96484,56 ąÜą╗ * 1 ą╝ąŠą╗čī = 1,3474e-7 ą╝ąŠą╗čī ąĄą╗ąĄą║čéčĆąŠąĮč¢ą▓. ąŚ čāčĆą░čģčāą▓ą░ąĮąĮčÅą╝ ą║ąŠąĄčäč¢čåč¢čöąĮčéč¢ą▓
ąÉąĮąŠą┤: 2H2 + 4OH– = 4H2O + 4e–
ąÜą░č鹊ą┤: O2 + 4e– + 2H2O = 4OH–
ą▓ąĖčģąŠą┤ąĖčéčī, čēąŠ ą║ąŠąČąĮčā čüąĄą║čāąĮą┤čā, ąĮą░ ą┐ąŠą▓ąĄčĆčģąĮč¢ ąĄą╗ąĄą║čéčĆąŠą┤čā ą┐ą╗ąŠčēąĄčÄ 1 čüą╝2 ą▓č¢ą┤ą▒čāą▓ą░čöčéčīčüčÅ ąĮą░ ą░ąĮąŠą┤č¢ ąŠą║ąĖčüąĮąĄąĮąĮčÅ 6,7368e-8 ą╝ąŠą╗čī ą▓ąŠą┤ąĮčÄ H2; ąĮą░ ą║ą░č鹊ą┤č¢ ą▓č¢ą┤ąĮąŠą▓ą╗ąĄąĮąĮčÅ 3,3684e-8 ą╝ąŠą╗čī ą║ąĖčüąĮčÄ O2.
ąĪąĖą╗ą░ čüčéčĆčāą╝čā ą▓ 13 ą╝č¢ą╗č¢ą░ą╝ą┐ąĄčĆ/čüą╝2 ąĘ ąĘąŠą▓ąĮč¢čłąĮčīąŠčŚ ą┐ą╗ąŠčēč¢ ąĄą╗ąĄą║čéčĆąŠą┤čā ąĘą░ąĮą░ą┤č鹊 ąĮąĖąĘčīą║ą░, čēąŠą▒ ąČąĖą▓ąĖčéąĖ ąĄą╗ąĄą║čéčĆąŠąĮąĮąĄ ąŠą▒ą╗ą░ą┤ąĮą░ąĮąĮčÅ, ą┐čĆąĖą▓ąŠą┤ąĖčéąĖ ą┤ąŠ čĆčāčģčā ąĄą╗ąĄą║čéčĆąĖčćąĮč¢ ą┤ą▓ąĖą│čāąĮąĖ. ąóąŠą╝čā ą┐ąĄčĆąĄą┤ ą┤ąŠčüą╗č¢ą┤ąĮąĖą║ą░ą╝ąĖ čüč鹊čÅą╗ą░ ąĘą░ą┤ą░čćą░ ą┐č¢ą┤ą▓ąĖčēąĖčéąĖ čüąĖą╗čā čüčéčĆčāą╝čā ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéčā ą┤ąŠ čüąŠč鹥ąĮčī ą╝č¢ą╗č¢ą░ą╝ą┐ąĄčĆ ąĘ čüą╝2.
ą»ą║ ą┐č¢ą┤ą▓ąĖčēąĖčéąĖ čüąĖą╗čā čüčéčĆčāą╝čā ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéčā?
- ą┐č¢ą┤ą▓ąĖčēąĖčéąĖ č鹥ą╝ą┐ąĄčĆą░čéčāčĆčā čüąĖčüč鹥ą╝ąĖ, ą░ą╗ąĄ ą╝ą░č鹥čĆč¢ą░ą╗ąĖ ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéčā č¢ ąĘą░ ą║č¢ą╝ąĮą░čéąĮąŠčŚ č鹥ą╝ą┐ąĄčĆą░čéčāčĆ ąĮąĄ ąĮą░ą┤č鹊 ą┤ąŠą▓ą│ąŠą▓č¢čćąĮč¢;
- ąĘą▒č¢ą╗čīčłąĖčéąĖ ą║č¢ą╗čīą║č¢čüčéčī ą░ą║čéč¢ą▓ ąĄą╗ąĄą║čéčĆąŠčģč¢ą╝č¢čćąĮąĖčģ čĆąĄą░ą║čåč¢ą╣, čłą╗čÅčģąŠą╝ ąĘą▒č¢ą╗čīčłąĄąĮąĮčÅ ą║ąŠąĮčåąĄąĮčéčĆą░čåč¢čŚ ą│ą░ąĘč¢ą▓, č鹊ą▒č鹊 ąĘą▒č¢ą╗čīčłčāčÄčćąĖ čéąĖčüą║ ą▓ čüąĖčüč鹥ą╝č¢;
- ąĘą▒č¢ą╗čīčłąĖčéąĖ ą▓ąĮčāčéčĆč¢čłąĮčÄ ą┐ą╗ąŠčēčā ą┐ąŠą▓ąĄčĆčģąĮč¢ ąĄą╗ąĄą║čéčĆąŠą┤čā.
ąóą░ą▒ą╗ąĄčéą║ą░ ą░ą║čéąĖą▓ąŠą▓ą░ąĮąŠą│ąŠ ą▓čāą│č¢ą╗ą╗čÅ ą╝ą░čö ą┤č¢ą░ą╝ąĄčéčĆ 1,10 čüą╝ č¢ ą▓ąĖčüąŠčéčā 0,40 čüą╝, ąĘąŠą▓ąĮč¢čłąĮčÅ ą┐ą╗ąŠčēą░ čéą░ą▒ą╗ąĄčéą║ąĖ ą░ą║čéąĖą▓ąŠą▓ą░ąĮąŠą│ąŠ ą▓čāą│č¢ą╗ą╗čÅ ą┤ąŠčĆč¢ą▓ąĮčÄčö 3,28 čüą╝2, ą░ą╗ąĄ ą▓ąĮčāčéčĆč¢čłąĮčÅ ą┐ą╗ąŠčēą░ ą┐ąŠą▓ąĄčĆčģąĮč¢ čéą░ą▒ą╗ąĄčéą║ąĖ ą░ą║čéąĖą▓ąŠą▓ą░ąĮąŠą│ąŠ ą▓čāą│č¢ą╗ą╗čÅ čüčÅą│ą░čö 4 ą╝č¢ą╗čīą╣ąŠąĮč¢ą▓ čüą╝2 (400 ą╝2). ą”ąĄ ą▓ 1,2 ą╝č¢ą╗čīą╣ąŠąĮą░ čĆą░ąĘč¢ą▓ ą▒č¢ą╗čīčłąĄ ąĘą░ ąĘąŠą▓ąĮč¢čłąĮčÄ ą┐ą╗ąŠčēčā ą┐ąŠą▓ąĄčĆčģąĮč¢.
ąöąŠčüą╗č¢ą┤ąĮąĖą║ąĖ ą▓ čüą▓ąŠčŚčģ ą┤ąŠčüą╗č¢ą┤ą░čģ ą┐č¢čłą╗ąĖ čłą╗čÅčģąŠą╝ ąĘą▒č¢ą╗čīčłąĄąĮąĮčÅ ą▓ąĮčāčéčĆč¢čłąĮčīąŠčŚ ą┐ą╗ąŠčēč¢ ą┐ąŠą▓ąĄčĆčģąĮč¢ ąĄą╗ąĄą║čéčĆąŠą┤č¢ą▓ ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéčā. ąÆąĮčāčéčĆč¢čłąĮčÄ ą┐ą╗ąŠčēčā ą┐ąŠą▓ąĄčĆčģąĮč¢ ąĘą▒č¢ą╗čīčłčāą▓ą░ą╗ąĖ čłą╗čÅčģąŠą╝ čüčéą▓ąŠčĆąĄąĮąĮčÅ ą┐ąŠčĆąĖčüčéąĖčģ ąĄą╗ąĄą║čéčĆąŠą┤č¢ą▓. ą¤čĆąŠą▒ą╗ąĄą╝ą░ ą┐ąŠčĆąĖčüčéąĖčģ ąĄą╗ąĄą║čéčĆąŠą┤č¢ą▓ ą┤ą╗čÅ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓ ą┐ąŠą╗čÅą│ą░čö ą▓ č鹊ą╝čā, čēąŠ ąĄą╗ąĄą║čéčĆąŠčģč¢ą╝č¢čćąĮč¢ čĆąĄą░ą║čåč¢čŚ ą┐čĆąŠčéč¢ą║ą░čÄčéčī ąĮą░ ą╝ąĄąČč¢ čéčĆčīąŠčģ čäą░ąĘ. ąóąŠą▒č鹊 ą┐ąŠčĆąĖčüčéąĖą╣ ąĄą╗ąĄą║čéčĆąŠą┤ ą┐ąŠčéčĆč¢ą▒ąĮąŠ ąĮąĄ ą┐čĆąŠčüč鹊 ąĘą░ą┐ąŠą▓ąĮąĖčéąĖ ąĄą╗ąĄą║čéčĆąŠą╗č¢č鹊ą╝, ą░ čēąĄ ą┤ąŠą┤ą░čéąĖ ą│ą░ąĘ, ąĘą░ą▒ąĄąĘą┐ąĄčćąĖčéąĖ ą┐čĆąĖą╣ąŠą╝ č¢ ą┐ąĄčĆąĄą┤ą░čćčā ąĄą╗ąĄą║čéčĆąŠąĮč¢ą▓ ą┤ąŠ ą┐čĆąŠą▓č¢ą┤ąĮąĖą║ą░, ą▓č¢ą┤ą▓ąŠą┤ąĖčéąĖ ą┐čĆąŠą┤čāą║čéąĖ ąĄą╗ąĄą║čéčĆąŠčģč¢ą╝č¢čćąĮąĖčģ čĆąĄą░ą║čåč¢ą╣ (ąĮą░ą┐čĆąĖą║ą╗ą░ą┤ ą▓ąŠą┤čā). ąĀąŠąĘą▓ŌĆÖčÅąĘą░ąĮąĮčÅ ą┐čĆąŠą▒ą╗ąĄą╝ąĖ ą┐ąŠą▒ą░čćąĖą╗ąĖ ą▓ čüčéą▓ąŠčĆąĄąĮąĮč¢ ą╝ąĄčĆąĄąČč¢ ą┐ąŠčĆ, ą║ą░ąĮą░ą╗č¢ą▓ čĆč¢ąĘąĮąĖčģ čéąĖą┐č¢ą▓. ąÆ ą╝ą░č鹥čĆč¢ą░ą╗č¢ ąĄą╗ąĄą║čéčĆąŠą┤čā ą┐ąŠčéčĆč¢ą▒ąĮąŠ ą▒čāą╗ąŠ čüčéą▓ąŠčĆąĖčéąĖ ą│č¢ą┤čĆąŠč乊ą▒ąĮč¢ (ąĮąĄ ąĘą╝ąŠčćčāčÄčéčīčüčÅ ą▓ąŠą┤ąŠčÄ) čéą░ ą│č¢ą┤čĆąŠčäč¢ą╗čīąĮč¢ (ąĘą╝ąŠčćčāčÄčéčīčüčÅ ą▓ąŠą┤ąŠčÄ) ą║ą░ąĮą░ą╗ąĖ, ą░ čéą░ą║ąŠąČ, čüą░ą╝ ą╝ą░č鹥čĆč¢ą░ą╗ ąĄą╗ąĄą║čéčĆąŠą┤čā ą┐ąŠą▓ąĖąĮąĄąĮ ą▒čāčéąĖ ąĄą╗ąĄą║čéčĆąŠą┐čĆąŠą▓č¢ą┤ąĮąĖą╝. ąōč¢ą┤čĆąŠč乊ą▒ąĮč¢ ą║ą░ąĮą░ą╗ąĖ ą┐čĆąŠą┐čāčüą║ą░čÄčéčī ą│ą░ąĘąĖ (ą▓ąŠą┤ąĄąĮčī čéą░ ą║ąĖčüąĄąĮčī), ą░ą╗ąĄ ąĮąĄ ą┐čĆąŠą┐čāčüą║ą░čÄčéčī ą▓ąŠą┤čā (ąĄą╗ąĄą║čéčĆąŠą╗č¢čé), ą│č¢ą┤čĆąŠčäč¢ą╗čīąĮč¢ ą║ą░ąĮą░ą╗ąĖ ąĮą░ą▓ą┐ą░ą║ąĖ – ąĘą░ą┐ąŠą▓ąĮčÄčÄčéčīčüčÅ ąĄą╗ąĄą║čéčĆąŠą╗č¢č鹊ą╝, ą░ą╗ąĄ ąĮąĄą┤ąŠčüčéčāą┐ąĮč¢ ą┤ą╗čÅ ą│ą░ąĘč¢ą▓.
ąÆąĖą┐čĆąŠą▒ąŠą▓čāą▓ą░ą╗ąĖ čĆč¢ąĘąĮč¢ ą▓ą░čĆč¢ą░ąĮčéąĖ čüčéą▓ąŠčĆąĄąĮąĮčÅ ą┐ąŠčĆąĖčüčéąĖčģ ąĄą╗ąĄą║čéčĆąŠą┐čĆąŠą▓č¢ą┤ąĮąĖčģ ą╝ą░č鹥čĆč¢ą░ą╗č¢ą▓. ąØą░ą┐čĆąĖą║ą╗ą░ą┤, ą▒čĆą░ą╗ąĖ ąĘą░ą╗č¢ąĘąĮčā čüč¢čéą║čā č¢ ąĘą░ą╗č¢ąĘąĮčā ą┐ą╗ą░čüčéąĖąĮčā ąĘ ąŠčéą▓ąŠčĆą░ą╝ąĖ, čÅą║č¢ čāčéą▓ąŠčĆčÄą▓ą░ą╗ąĖ ąŠčüąĮąŠą▓čā ąĄą╗ąĄą║čéčĆąŠą┤čā. ąØą░ čåčÄ ąŠčüąĮąŠą▓čā ąĮą░ą┐čĆąĄčüąŠą▓čāą▓ą░ą╗ąĖ ą░ą║čéąĖą▓ąĮčā ą╝ą░čüčā – čüčāą╝č¢čł ą▓čāą│č¢ą╗ą╗čÅ (ą│č¢ą┤čĆąŠčäč¢ą╗čīąĮąĖą╣ ą║ąŠą╝ą┐ąŠąĮąĄąĮčé) č¢ ą║ą░čāčćčāą║čā (ą│č¢ą┤čĆąŠč乊ą▒ąĮąĖą╣ ą║ąŠą╝ą┐ąŠąĮąĄąĮčé), ą┤ą╗čÅ ą┐ąŠą║čĆą░čēąĄąĮąĮčÅ ą│č¢ą┤čĆąŠč乊ą▒ąĮąĖčģ ą▓ą╗ą░čüčéąĖą▓ąŠčüč鹥ą╣ ą┤ąŠ čüčāą╝č¢čłč¢ ą┤ąŠą┤ą░ą▓ą░ą╗ąĖ ą┐ą░čĆą░čäč¢ąĮ. ąóą░ą║ąĖą╣ ąĄą╗ąĄą║čéčĆąŠą┤ ąĮąĄ ą╝č¢čüčéąĖą▓ ą┤ąŠčĆąŠą│ąŠčåč¢ąĮąĮąĖčģ ą╝ąĄčéą░ą╗č¢ą▓ č¢ ą║ą░čéą░ą╗č¢ąĘą░č鹊čĆč¢ą▓, č¢ ą▓ąĖą┤ą░ą▓ą░ą▓ ą┤ąŠčüčéą░čéąĮčīąŠ ą┐ąŠčéčāąČąĮąĖą╣ čüčéčĆčāą╝, ą░ą╗ąĄ ąĄą╗ąĄą║čéčĆąŠą┤ ą┤čāąČąĄ čłą▓ąĖą┤ą║ąŠ čĆčāą╣ąĮčāą▓ą░ą▓čüčÅ.
ąæčāą╗ąŠ ą┐čĆąŠą▓ąĄą┤ąĄąĮąŠ ą▒ą░ą│ą░č鹊 ąĄą║čüą┐ąĄčĆąĖą╝ąĄąĮčéč¢ą▓ č¢ ą┤ąŠčüą╗č¢ą┤ąČąĄąĮčī, ąŠčéčĆąĖą╝ą░ąĮąŠ ą┤ąŠą▓ąŠą╗č¢ ą▓ąĖčüąŠą║č¢ ą┐ąŠą║ą░ąĘąĮąĖą║ąĖ ą┐ąŠ čüąĖą╗č¢ čüčéčĆčāą╝čā ąĘ ą║ą▓ą░ą┤čĆą░čéąĮąŠą│ąŠ čüą░ąĮčéąĖą╝ąĄčéčĆčā, ą░ą╗ąĄ ąĮąĄą┤ąŠą▓ą│ąŠą▓č¢čćąĮč¢čüčéčī čüčéą▓ąŠčĆąĄąĮąĖčģ ąĘčĆą░ąĘą║č¢ą▓ ą┐ąŠčĆąĖčüčéąĖčģ ąĄą╗ąĄą║čéčĆąŠą┤č¢ą▓ ąĮąĄ ą┤ąŠąĘą▓ąŠą╗ąĖą╗ą░ ą▓ąĖą║ąŠčĆąĖčüč鹊ą▓čāą▓ą░čéąĖ č鹥čģąĮąŠą╗ąŠą│č¢čÄ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓ ą▓ ą┐čĆąŠą╝ąĖčüą╗ąŠą▓ąŠčüčéč¢ čéą░ ą┐ąŠą▒čāčéč¢.
ą¤ąŠčéčĆč¢ą▒ąĄąĮ ą▒čāą▓ č¢ąĮąĄčĆčéąĮąĖą╣, čüčéč¢ą╣ą║ąĖą╣ ą┤ąŠ ą░ą│čĆąĄčüąĖą▓ąĮąĖčģ čüąĄčĆąĄą┤ąŠą▓ąĖčē čéą░ ą▓ąĖčüąŠą║ąĖčģ č鹥ą╝ą┐ąĄčĆą░čéčāčĆ ą│č¢ą┤čĆąŠč乊ą▒ąĮąĖą╣ ą╝ą░č鹥čĆč¢ą░ą╗.
ąÆ 70-čģ čĆąŠą║ą░čģ ąźąź čüčé. čéą░ą║ąĖą╣ ą╝ą░č鹥čĆč¢ą░ą╗ ą▒čāą╗ąŠ ąĘąĮą░ą╣ą┤ąĄąĮąŠ – č鹥čäą╗ąŠąĮ.
ążč鹊čĆąŠą┐ą╗ą░čüčé-4, ą░ą▒ąŠ ą┐ąŠą╗č¢č鹥čéčĆą░čäą╗čāąŠčĆąĄč鹥ąĮ, ą░ą▒ąŠ č鹥čäą╗ąŠąĮ, -(CF2-CF2)-. ąóąĄčäą╗ąŠąĮ ąĮą░ą┤ąĘą▓ąĖčćą░ą╣ąĮąŠ čüčéč¢ą╣ą║ąĖą╣ ą┤ąŠ ą░ą│čĆąĄčüąĖą▓ąĮąĖčģ čüąĄčĆąĄą┤ąŠą▓ąĖčē, ą║ąĖčüą╗ąŠčéąĖ (ąĮą░ą▓č¢čéčī čåą░čĆčüčīą║ą░ ą▓ąŠą┤ą║ą░), ą╗čāą│ąĖ čéą░ ąŠą║ąĖčüąĮąĖą║ąĖ ąĮą░ č鹥čäą╗ąŠąĮ ąĮąĄ ą┤č¢čÄčéčī. ąöč¢ą░ą┐ą░ąĘąŠąĮ čĆąŠą▒ąŠčćąĖčģ č鹥ą╝ą┐ąĄčĆą░čéčāčĆ č鹥čäą╗ąŠąĮčā ą▓č¢ą┤ -250*ąĪ ą┤ąŠ +250*ąĪ. ąóąĄčäą╗ąŠąĮ ąĮąĄ čéč¢ą╗čīą║ąĖ ąĮą░ą┤ąĘą▓ąĖčćą░ą╣ąĮąŠ ą│č¢ą┤čĆąŠč乊ą▒ąĮąĖą╣ ą╝ą░č鹥čĆč¢ą░ą╗, ą▓č¢ąĮ čéą░ą║ąŠąČ ąĮąĄ ąĘą╝ąŠčćčāčöčéčīčüčÅ ą░ąĮč¢ ąČąĖčĆą░ą╝ąĖ, ą░ąĮč¢ ą▒č¢ą╗čīčłč¢čüčéčÄ ąŠčĆą│ą░ąĮč¢čćąĮąĖčģ čĆąŠąĘčćąĖąĮąĮąĖą║č¢ą▓.
ąĪą░ą╝ąĄ čäč鹊čĆąŠą┐ą╗ą░čüčé ą┐ąŠčćą░ą╗ąĖ ą▓ąĖą║ąŠčĆąĖčüč鹊ą▓čāą▓ą░čéąĖ ą┐čĆąĖ čüčéą▓ąŠčĆąĄąĮąĮč¢ ą┐ąŠčĆąĖčüčéąĖčģ ąĄą╗ąĄą║čéčĆąŠą┤č¢ą▓ ą┤ą╗čÅ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓, ąĘą╝č¢čłčāčÄčćąĖ ą┐ąŠčĆąŠčłąŠą║ č鹥čäą╗ąŠąĮčā ąĘ ą┐ąŠčĆąŠčłą║ą░ą╝ąĖ ą╝ąĄčéą░ą╗č¢ą▓. ąŚą░ą▓ą┤čÅą║ąĖ ą▓ą╗ą░čüčéąĖą▓ąŠčüčéčÅą╝ čäč鹊čĆąŠą┐ą╗ą░čüčéčā, ą┐ą░ą╗ąĖą▓ąĮč¢ ąĄą╗ąĄą╝ąĄąĮčéąĖ ąŠčéčĆąĖą╝ą░ą╗ąĖ ąĮąŠą▓ąĖą╣ čłą░ąĮčü ąĮą░ ąĘą░ą│ą░ą╗čīąĮąĄ ąĘą░čüč鹊čüčāą▓ą░ąĮąĮčÅ ą▓ ą┐čĆąŠą╝ąĖčüą╗ąŠą▓ąŠčüčéč¢ čéą░ ą┐ąŠą▒čāčéč¢.
ąÆą┤ąŠčüą║ąŠąĮą░ą╗ąĄąĮąĮčÅ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓ ą┤ąŠąĘą▓ąŠą╗ąĖą╗ąŠ čüčéą▓ąŠčĆąĖčéąĖ ą┤ąĄą╝ąŠąĮčüčéčĆą░čåč¢ą╣ąĮč¢ ą┐čĆąŠč鹊čéąĖą┐ąĖ ą┐čĆąĖčüčéčĆąŠčŚą▓, ą┤ą╗čÅ čĆąŠą▒ąŠčéąĖ čÅą║ąĖčģ ą┤ąČąĄčĆąĄą╗ąŠą╝ ąĄąĮąĄčĆą│č¢čŚ ą▒čāą╗ąĖ ą┐ą░ą╗ąĖą▓ąĮč¢ ąĄą╗ąĄą╝ąĄąĮčéąĖ.
ąóą░ą║, ą▓ 1965 čĆąŠčåč¢, ąĮč¢ą╝ąĄčåčīą║ą░ čäč¢čĆą╝ą░ ŌĆ£ąĪč¢ą╝ąĄąĮčüŌĆØ čüčéą▓ąŠčĆąĖą╗ą░ ą┐čĆąŠč鹊čéąĖą┐ ą╝ąŠč鹊čĆąĮąŠą│ąŠ č湊ą▓ąĮą░, ąĘ ą┐ą░ą╗ąĖą▓ąĮąĖą╝ ąĄą╗ąĄą╝ąĄąĮč鹊ą╝ ą┐ąŠčéčāąČąĮč¢čüčéčÄ 0,5 ą║ąÆčé. ą¦ąŠą▓ąĄąĮ ą▒čāą╗ąŠ čĆąŠąĘčĆą░čģąŠą▓ą░ąĮąŠ ąĮą░ 5 ąŠčüč¢ą▒ č¢ čĆčāčģą░ą▓čüčÅ ą▓č¢ąĮ ąĘč¢ čłą▓ąĖą┤ą║č¢čüčéčÄ 7 ą║ą╝/ą│ąŠą┤.
ąÆ 60-čģ čĆąŠą║ą░čģ ąźąź čüčé., ą░ą╝ąĄčĆąĖą║ą░ąĮčüčīą║ą░ ą║ąŠą╝ą┐ą░ąĮč¢čÅ ŌĆ£ą«ąĮč¢ąŠąĮ ą║ą░čĆą▒ą░ą╣ą┤ŌĆØ ąĮą░ ąĘą░ą╝ąŠą▓ą╗ąĄąĮąĮčÅ ŌĆ£ąöąČąĄąĮąĄčĆą░ą╗ ą╝ąŠč鹊čĆčüŌĆØ čĆąŠąĘčĆąŠą▒ąĖą╗ą░ ąĄąĮąĄčĆą│ąŠčüąĖčüč鹥ą╝čā ą┤ą╗čÅ ąĮąĄą▓ąĄą╗ąĖą║ąŠą│ąŠ ąĄą║čüą┐ąĄčĆąĖą╝ąĄąĮčéą░ą╗čīąĮąŠą│ąŠ ąĄą╗ąĄą║čéčĆąŠą╝ąŠą▒č¢ą╗čÄ ą┐č¢ą┤ ąĮą░ąĘą▓ąŠčÄ ŌĆ£ąĢą╗ąĄą║čéčĆąŠą▓ą░ąĮŌĆØ. ąĀąŠą▒ąŠčćą░ ą┐ąŠčéčāąČąĮč¢čüčéčī ą▒ą░čéą░čĆąĄčŚ ąĮą░ ą▓ąŠą┤ąĮąĄą▓ąŠ-ą║ąĖčüąĮąĄą▓ąĖčģ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéą░čģ čüčéą░ąĮąŠą▓ąĖą╗ą░ 32 ą║ąÆčé, ą╝ą░ą║čüąĖą╝ą░ą╗čīąĮąŠ ą╝ąŠąČą╗ąĖą▓ą░ ą┐ąŠčéčāąČąĮč¢čüčéčī 160 ą║ąÆčé. ąÆąŠą┤ąĄąĮčī č¢ ą║ąĖčüąĄąĮčī ąĘą▒ąĄčĆč¢ą│ą░ą╗ąĖčüčÅ ą▓ ąĘčĆč¢ą┤ąČąĄąĮąŠą╝čā čüčéą░ąĮč¢ ą▓ ą▒ą░ą╗ąŠąĮą░čģ. ą¤čĆąĖ ą┐ąŠčéčāąČąĮąŠčüčéč¢ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓ 90 ą║ąÆčé ŌĆ£ąĢą╗ąĄą║čéčĆąŠą▓ą░ąĮŌĆØ čĆąŠąĘą▓ąĖą▓ą░ą▓ čłą▓ąĖą┤ą║č¢čüčéčī 80 ą║ą╝/ą│ąŠą┤ (ą╝ą░ą║čüąĖą╝ą░ą╗čīąĮą░ čłą▓ąĖą┤ą║č¢čüčéčī ą▒čāą╗ą░ 114 ą║ą╝/ą│ąŠą┤). ąÆ ąĘą░ą╗ąĄąČąĮąŠčüčéč¢ ą▓č¢ą┤ ąĮą░ą▓ą░ąĮčéą░ąČąĄąĮąĮčÅ ŌĆ£ąĢą╗ąĄą║čéčĆąŠą▓ą░ąĮŌĆØ ą╝č¢ą│ ą┐čĆąŠčŚčģą░čéąĖ ą▓č¢ą┤čüčéą░ąĮčī ą▓č¢ą┤ 160 ą┤ąŠ 240 ą║č¢ą╗ąŠą╝ąĄčéčĆč¢ą▓ ąĮą░ 5,5 ą║ą│ čĆč¢ą┤ą║ąŠą│ąŠ ą▓ąŠą┤ąĮčÄ č¢ 45 ą║ą│ čĆč¢ą┤ą║ąŠą│ąŠ ą║ąĖčüąĮčÄ.
ąÆ čéč¢ ąČ čĆąŠą║ąĖ ą▓ ąĪą©ąÉ ą▒čāą╗ąŠ čĆąŠąĘčĆąŠą▒ą╗ąĄąĮąŠ ą┐č¢ą┤ą▓ąŠą┤ąĮąĖą╣ č湊ą▓ąĄąĮ (ą┤ąŠčüą╗č¢ą┤ąĮąĖčåčīą║ąŠ-ą┐ąŠčłčāą║ąŠą▓ąŠą│ąŠ čéąĖą┐čā), ąĮą░ 4 ąŠčüąŠą▒ąĖ, čÅą║ąĖą╣ ą╝č¢ą│ ąĘą░ąĮčāčĆčÄą▓ą░čéąĖčüčÅ ąĮą░ ą│ą╗ąĖą▒ąĖąĮčā ą┤ąŠ 6 ą║ą╝. ą¦ąŠą▓ąĄąĮ ą▒čāą╗ąŠ ąŠčüąĮą░čēąĄąĮąŠ ą▒ą░čéą░čĆąĄčöčÄ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓ čäč¢čĆą╝ąĖ ŌĆ£ą«ąĮč¢ąŠąĮ ą║ą░čĆą▒ą░ą╣ą┤ŌĆØ, ą┐ąŠčéčāąČąĮč¢čüčéčÄ 25-50 ą║ąÆčé, ąÜąÜąö ąĄąĮąĄčĆą│ąĄčéąĖčćąĮąŠčŚ čāčüčéą░ąĮąŠą▓ą║ąĖ 58%.
ą¤čĆąŠč鹥, ąĮą░ čłą╗čÅčģčā ą┤ąŠ ąĘą░ą│ą░ą╗čīąĮąŠą│ąŠ ą╝ą░čüąŠą▓ąŠą│ąŠ ą▓ąĖą║ąŠčĆąĖčüčéą░ąĮąĮčÅ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓ ą▒čāą╗ąŠ ą▒ą░ą│ą░č鹊 ą┐čĆąŠą▒ą╗ąĄą╝.
ąÉą╗čīč鹥čĆąĮą░čéąĖą▓ąĮč¢ ą┐ą░ą╗ąĖą▓ąĮč¢ ąĄą╗ąĄą╝ąĄąĮčéąĖ
ąØą░ą╣ą║čĆą░čēč¢ čĆąĄąĘčāą╗čīčéą░čéąĖ ą┐ąŠ ąĄč乥ą║čéąĖą▓ąĮąŠčüčéč¢ ą╝ą░čö ą┐ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé ąĮą░ čćąĖčüčéąĖčģ ą▓ąŠą┤ąĮč¢ čéą░ ą║ąĖčüąĮč¢. ąÉą╗ąĄ čåč¢ ą│ą░ąĘąĖ (ąŠčüąŠą▒ą╗ąĖą▓ąŠ ą▓ąŠą┤ąĄąĮčī) ąŠčéčĆąĖą╝ą░čéąĖ č¢ ąŠčćąĖčüčéąĖčéąĖ ąĮąĄą╗ąĄą│ą║ąŠ, čēąŠ čüčāčéčéčöą▓ąŠ ąĘą▒č¢ą╗čīčłčāčö čŚčģ čåč¢ąĮčā. ąöą╗čÅ ą╝ą░čüąŠą▓ąŠą│ąŠ ą▓ąĖą║ąŠčĆąĖčüčéą░ąĮąĮčÅ ą┐ąŠčéčĆč¢ą▒ąĮąŠ čüčéą▓ąŠčĆąĖčéąĖ ąĄč乥ą║čéąĖą▓ąĮč¢ č¢ ąĮą░ą┤č¢ą╣ąĮč¢ ą┐ą░ą╗ąĖą▓ąĮč¢ ąĄą╗ąĄą╝ąĄąĮčéąĖ, čÅą║č¢ ą┐čĆą░čåčÄą▓ą░čéąĖą╝čāčéčī ąĮą░ ą┤ąĄčłąĄą▓ąŠą╝čā č¢ ą┤ąŠčüčéčāą┐ąĮąŠą╝čā ą┐ą░ą╗ąĖą▓č¢ (ą┐čĆąĖčĆąŠą┤ąĮąĖą╣ ą│ą░ąĘ, čüą┐ąĖčĆčéąĖ, ą▒ąĄąĮąĘąĖąĮ, č¢ č¢ąĮčłč¢), ą░ ą▓ čÅą║ąŠčüčéč¢ ąŠą║ąĖčüąĮčÄą▓ą░čćą░ ąĮąĄąŠą▒čģč¢ą┤ąĮąŠ ą▓ąĖą║ąŠčĆąĖčüč鹊ą▓čāą▓ą░čéąĖ ą║ąĖčüąĄąĮčī ą┐ąŠą▓č¢čéčĆčÅ.
ąÆ čÅą║ąŠčüčéč¢ ą░ą╗čīč鹥čĆąĮą░čéąĖą▓ąĖ ą▓ąŠą┤ąĄąĮčī-ą║ąĖčüąĮąĄą▓ąŠą╝čā ą┐ą░ą╗ąĖą▓ąĮąŠą╝čā ąĄą╗ąĄą╝ąĄąĮčéčā, ą▓ 1964 čĆąŠčåč¢ ą▓ ą╝. ąōčĆąŠč鹊ąĮ (ąĪą©ąÉ) ą▒čāą╗ąŠ čüčéą▓ąŠčĆąĄąĮąŠ ąŠą┤ąĮąŠą╝č¢čüąĮąĖą╣ ą┐č¢ą┤ą▓ąŠą┤ąĮąĖą╣ č湊ą▓ąĄąĮ ŌĆ£StartŌĆØ (ą┤ąŠą▓ąČąĖąĮąŠčÄ 3 ą╝ąĄčéčĆąĖ č¢ ą╝ą░čüąŠčÄ 1 č鹊ąĮąĮą░) ąŠčüąĮą░čēąĄąĮąĖą╣ ą│č¢ą┤čĆą░ąĘąĖąĮ-ą║ąĖčüąĮąĄą▓ąĖą╝ ą┐ą░ą╗ąĖą▓ąĮąĖą╝ ąĄą╗ąĄą╝ąĄąĮč鹊ą╝ ą┐ąŠčéčāąČąĮč¢čüčéčÄ 0,750 ą║ąÆčé.
N2H4 + O2 = N2 + 2H2O
N2H4 + 4OH– = N2 + 2H2O + 4e–
ąæą░čéą░čĆąĄčÅ ąĘą░ą▒ąĄąĘą┐ąĄčćčāą▓ą░ą╗ą░ čĆąŠą▒ąŠčéčā č湊ą▓ąĮą░ ą┐čĆąŠčéčÅą│ąŠą╝ 12 ą│ąŠą┤ąĖąĮ: čĆčāčģ, ąĘą░ąĮčāčĆąĄąĮąĮčÅ ąĮą░ ą│ą╗ąĖą▒ąĖąĮčā ą┤ąŠ 90 ą╝, ąŠčüą▓č¢čéą╗ąĄąĮąĮčÅ, čĆą░ą┤č¢ąŠąĘą▓ŌĆÖčÅąĘąŠą║, ąĘą░čüąŠą▒ąĖ ąĮą░ą▓č¢ą│ą░čåč¢čŚ.
ą”č¢ąĮą░ ą│č¢ą┤čĆą░ąĘąĖąĮčā ą▓ 15-20 čĆą░ąĘč¢ą▓ ą▒č¢ą╗čīčłą░ ąĘą░ čåč¢ąĮčā ą▓ąŠą┤ąĮčÄ. ąōč¢ą┤čĆą░ąĘąĖąĮ č鹊ą║čüąĖčćąĮąĖą╣. ąóąŠą╝čā ą╣ąŠą│ąŠ ą▓ąĖą║ąŠčĆąĖčüčéą░ąĮąĮčÅ ą▓ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéą░čģ ąŠą▒ą╝ąĄąČąĖą╗ąŠčüčÅ ą╗ąĖčłąĄ ą┤ąĄą╝ąŠąĮčüčéčĆą░čåč¢ą╣ąĮąĖą╝ąĖ ąĘčĆą░ąĘą║ą░ą╝ąĖ.
ąÉą╝ąŠąĮč¢ą░ą║ č鹥ąČ ą╝ąŠąČąĮą░ ą▓ąĖą║ąŠčĆąĖčüč鹊ą▓čāą▓ą░čéąĖ ą▓ čÅą║ąŠčüčéč¢ ą┐ą░ą╗ąĖą▓ą░ ą▓ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéą░čģ. ą”č¢ąĮą░ ą░ą╝ąŠąĮč¢ą░ą║čā čéą░ą║ą░ čüą░ą╝ą░ čÅą║ č¢ ą▓ąŠą┤ąĮčÄ, ą░ą╗ąĄ ą░ą╝ąŠąĮč¢ą░ą║ ą┐ąŠčüčéčāą┐ą░čöčéčīčüčÅ ą▓ąŠą┤ąĮčÄ ąĘą░ čĆąĄą░ą║čåč¢ą╣ąĮąŠčÄ ąĘą┤ą░čéąĮč¢čüčéčÄ. ąØąĖąĘčīą║čā čĆąĄą░ą║čåč¢ą╣ąĮčā ąĘą┤ą░čéąĮč¢čüčéčī ą╝ą░čö, ą╝ąĄčéą░ąĮąŠą╗ č¢ č¢ąĮčłč¢ čüą┐ąĖčĆčéąĖ.
ąÆ 1962 čĆąŠčåč¢ ą░ą╝ąĄčĆąĖą║ą░ąĮčüčīą║ąĖą╣ ąĄą╗ąĄą║čéčĆąŠčģč¢ą╝č¢ą║ ąØč¢ą┤čĆą░čģ ą▓ąĖčÅą▓ąĖą▓, čēąŠ ą┐čĆąĖ 25*ąĪ ąĮą░ ąĄą╗ąĄą║čéčĆąŠą┤ą░čģ ą▓ąĖą│ąŠč鹊ą▓ą╗ąĄąĮąĖčģ ąĘ ą┤čĆč¢ą▒ąĮąŠą┤ąĖčüą┐ąĄčĆčüąĮąŠčŚ ą┐ą╗ą░čéąĖąĮąĖ ą╣ą┤ąĄ ąĄą╗ąĄą║čéčĆąŠčģč¢ą╝č¢čćąĮąĄ ąŠą║ąĖčüąĮąĄąĮąĮčÅ ąĄčéą░ąĮčā. ąĢą╗ąĄą║čéčĆąŠčģč¢ą╝č¢čćąĮąĖą╣ ą┐čĆąŠčåąĄčü ą┤ą░ą▓ą░ą▓ ą╗ąĖčłąĄ 5 ą╝č¢ą╗č¢ą░ą╝ą┐ąĄčĆ ąĮą░ čüą░ąĮčéąĖą╝ąĄčéčĆ ą║ą▓ą░ą┤čĆą░čéąĮąĖą╣ ą┐ąŠą▓ąĄčĆčģąĮč¢ ąĄą╗ąĄą║čéčĆąŠą┤čā. ą¤ąŠą┤ą░ą╗čīčłč¢ ą┤ąŠčüą╗č¢ą┤ąĖ ąĘ ą║ą░čĆą▒ąŠą│č¢ą┤čĆąŠą│ąĄąĮą░ą╝ąĖ ą┐ąŠą║ą░ąĘą░ą╗ąĖ, čēąŠ ą▓ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéą░čģ ą╝ąŠąČąĮą░ čüą┐ą░ą╗čÄą▓ą░čéąĖ ą▓čüč¢ ą│ą░ąĘąŠą┐ąŠą┤č¢ą▒ąĮč¢ ą║ą░čĆą▒ąŠą│č¢ą┤čĆąŠą│ąĄąĮąĖ, ą┐ąŠą▓ąĮč¢čüčéčÄ, ą┤ąŠ ą║ą░čĆą▒ąŠąĮ ą┤č¢ąŠą║čüąĖą┤čā č¢ ą▓ąŠą┤ąĖ. ąÉą╗ąĄ čĆąĄą░ą╗č¢ąĘčāą▓ą░čéąĖ čüą┐ą░ą╗ąĄąĮąĮčÅ ą│ą░ąĘąŠą┐ąŠą┤č¢ą▒ąĮąĖčģ ą║ą░čĆą▒ąŠą│č¢ą┤čĆąŠą│ąĄąĮč¢ą▓ ą▓ ą┐čĆąŠą╝ąĖčüą╗ąŠą▓ąĖčģ ą╝ą░čüčłčéą░ą▒ą░čģ ąĮąĄ ą▓ąĖą╣čłą╗ąŠ. ą×čüąĮąŠą▓ąĮąŠčÄ ą┐čĆąŠą▒ą╗ąĄą╝ąŠčÄ ą┐čĆąĖ ą▓ąĖą║ąŠčĆąĖčüčéą░ąĮąĮč¢ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓ ą▓ ą┐čĆąŠą╝ąĖčüą╗ąŠą▓ąĖčģ ą╝ą░čüčłčéą░ą▒ą░čģ ąĮą░ ą│ą░ąĘąŠą┐ąŠą┤č¢ą▒ąĮąĖčģ ą║ą░čĆą▒ąŠą│č¢ą┤čĆąŠą│ąĄąĮą░čģ ą▒čāą╗ąŠ ą▓ąĖą║ąŠčĆąĖčüčéą░ąĮąĮčÅ ą┐ą╗ą░čéąĖąĮąŠą▓ąĖčģ ą║ą░čéą░ą╗č¢ąĘą░č鹊čĆč¢ą▓ ą▓ ąĄą╗ąĄą║čéčĆąŠą┤ą░čģ. ąóąŠą╝čā ą┤ąŠčüą╗č¢ą┤ąĮąĖą║ąĖ ą┐čĆą░čåčÄą▓ą░ą╗ąĖ ąĮą░ą┤ ą┐ąŠčłčāą║ąŠą╝ ąĮąŠą▓ąĖčģ ąĄč乥ą║čéąĖą▓ąĮąĖčģ ą║ą░čéą░ą╗č¢ąĘą░č鹊čĆč¢ą▓, čÅą║č¢ ą▒ ąĮąĄ ą╝č¢čüčéąĖą╗ąĖ ą┐ą╗ą░čéąĖąĮąĖ, ą░ą▒ąŠ ąĘąĮąĖąČčāą▓ą░ą╗ąĖ ą▒ čŚčŚ ą▓ąĖą║ąŠčĆąĖčüčéą░ąĮąĮčÅ.
ą¦ąĖčüą╗ąĄąĮąĮč¢ ąĄą║čüą┐ąĄčĆąĖą╝ąĄąĮčéąĖ ąĘ ą┐ąŠčłčāą║čā ąĮąŠą▓ąĖčģ ąĄą╗ąĄą║čéčĆąŠą║ą░čéą░ą╗č¢čéąĖčćąĮąĖčģ ą╝ą░č鹥čĆč¢ą░ą╗č¢ą▓ č¢ąĮąŠą┤č¢ ą┤ą░ą▓ą░ą╗ąĖ ąŠą▒ąĮą░ą┤č¢ą╣ą╗ąĖą▓č¢ čĆąĄąĘčāą╗čīčéą░čéąĖ.
ąÆ 1965 čĆąŠčåč¢ ą▒čāą╗ąŠ ą▓č¢ą┤ą║čĆąĖč鹊 ąĮąĄą▓č¢ą┤ąŠą╝č¢ čĆą░ąĮč¢čłąĄ ąĄą╗ąĄą║čéčĆąŠą║ą░čéą░ą╗č¢čéąĖčćąĮč¢ ąĄč乥ą║čéąĖ. ąØą░ą┐čĆąĖą║ą╗ą░ą┤, ąŠą║ąĖčüąĮąĄąĮąĮčÅ ą╝ąĄčéą░ąĮąŠą╗čā ąĮą░ ą┐ą╗ą░čéąĖąĮąŠ-čĆčāč鹥ąĮč¢čöą▓ąŠą╝čā ąĄą╗ąĄą║čéčĆąŠą┤č¢ ą▓č¢ą┤ą▒čāą▓ą░ą╗ąŠčüčÅ ą▓ čéąĖčüčÅčćč¢ čĆą░ąĘč¢ą▓ čłą▓ąĖą┤čłąĄ ąĮč¢ąČ ąĮą░ ą┐ą╗ą░čéąĖąĮąŠą▓ąŠą╝čā ąĄą╗ąĄą║čéčĆąŠą┤č¢.
ąÆ čģąŠą┤č¢ ąĄą║čüą┐ąĄčĆąĖą╝ąĄąĮčéč¢ą▓ ą▓ąĖčÅą▓ąĖą╗ąĖ, čēąŠ ą║ą░čĆą▒č¢ą┤ ą▓ąŠą╗čīčäčĆą░ą╝čā ą┐čĆąĄą║čĆą░čüąĮąŠ ą░ą┤čüąŠčĆą▒čāčö ą▓ąŠą┤ąĄąĮčī, ą▓č¢ąĮ č¢ąĮąĄčĆčéąĮąĖą╣ ą┐ąŠ ą▓č¢ą┤ąĮąŠčłąĄąĮąĮčÄ ą┤ąŠ ą║ąĖčüą╗ąŠčé.
ąØč¢ą╝ąĄčåčīą║ąĖą╣ čäč¢ąĘąĖą║ąŠ-čģč¢ą╝č¢ą║ ąĢ. ą«čüčéč¢ ąĘą░ą╝č¢ąĮąĖą▓ ą┐ą╗ą░čéąĖąĮąŠą▓ąĖą╣ ąĄą╗ąĄą║čéčĆąŠą┤ ą▓ ą▓ąŠą┤ąĮąĄą▓ąŠ-ą║ąĖčüąĮąĄą▓ąŠą╝čā ą┐ą░ą╗ąĖą▓ąĮąŠą╝čā ąĄą╗ąĄą╝ąĄąĮčéč¢ ąĮą░ čüą║ąĄą╗ąĄčéąĮąĖą╣ ą║ą░čéą░ą╗č¢ąĘą░č鹊čĆ (čüą┐ą╗ą░ą▓ ą╝ąĄčéą░ą╗čā-ą║ą░čéą░ą╗č¢ąĘą░č鹊čĆą░ ąĘ ą░ą╗čÄą╝č¢ąĮč¢čöą╝ ąĘ ą┐ąŠą┤ą░ą╗čīčłąĖą╝ čĆąŠąĘčćąĖąĮąĄąĮąĮčÅą╝ ą░ą╗čÄą╝č¢ąĮč¢čÄ ą▓ ą╗čāą│ą░čģ; čāčéą▓ąŠčĆčÄčöčéčīčüčÅ ą║ą░čéą░ą╗č¢čéąĖčćąĮąŠ ą░ą║čéąĖą▓ąĮą░ ą┐ąŠčĆąĖčüčéą░ ą╝ąĄčéą░ą╗ąĄą▓ą░ ą╝ą░čüą░).
ąÆ ą┐čĆąŠčåąĄčüč¢ ą┐ąŠčłčāą║č¢ą▓ ąĄč乥ą║čéąĖą▓ąĮąĖčģ ą║ą░čéą░ą╗č¢ąĘą░č鹊čĆč¢ą▓ ą┤ą╗čÅ ą▓ąĖą║ąŠčĆąĖčüčéą░ąĮąĮčÅ ą▓ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéą░čģ, čāą▓ą░ą│čā ąĄą╗ąĄą║čéčĆąŠčģč¢ą╝č¢ą║č¢ą▓ ą┐čĆąĖą▓ąĄčĆąĮčāą╗ąĖ ąŠčĆą│ą░ąĮč¢čćąĮč¢ čüą┐ąŠą╗čāą║ąĖ ą┐čĆąĖčĆąŠą┤ąĮąŠą│ąŠ ą┐ąŠčģąŠą┤ąČąĄąĮąĮčÅ ą┐ąŠčĆčäč¢čĆąĖąĮąĖ:
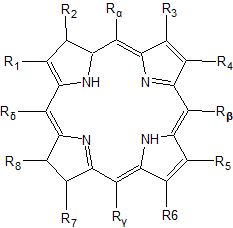
ą¤ąŠčĆčäč¢čĆąĖąĮąĖ čāčéą▓ąŠčĆčÄčÄčéčī ąĘ ą╝ąĄčéą░ą╗ą░ą╝ąĖ čģąĄą╗ą░čéąĮč¢ čüą┐ąŠą╗čāą║ąĖ č¢ ąĮą░ą▒čāą▓ą░čÄčéčī ą┐ąĄą▓ąĮąĖčģ ą║ą░čéą░ą╗č¢čéąĖčćąĮąĖčģ ą▓ą╗ą░čüčéąĖą▓ąŠčüč鹥ą╣. ą©čéčāčćąĮąŠ ą▒čāą╗ąŠ ąŠčéčĆąĖą╝ą░ąĮąŠ čüčéčĆčāą║čéčāčĆčā čüčģąŠąČčā ąĮą░ ą┐čĆąĖčĆąŠą┤ąĮč¢ ą┐ąŠčĆčäč¢čĆąĖąĮąĖ – čäčéą░ą╗ąŠčåąĖą░ąĮč¢ąĮ
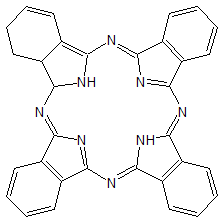
ążčéą░ą╗ąŠčåąĖą░ąĮč¢ąĮ ą▒č¢ą╗čīčł čüčéč¢ą╣ą║ąĖą╣ ą┤ąŠ č鹥ą╝ą┐ąĄčĆą░čéčāčĆ čéą░ čüą▓č¢čéą╗ą░, ą▒č¢ą╗čīčł č¢ąĮąĄčĆčéąĮąĖą╣ ą┤ąŠ ą║ąĖčüą╗ąŠčé čéą░ ą╗čāą│č¢ą▓, ąĮč¢ąČ ą┐čĆąĖčĆąŠą┤ąĮč¢ ą┐ąŠčĆčäč¢čĆąĖąĮąĖ. ąĪčīąŠą│ąŠą┤ąĮč¢ ą╗ą░ą▒ąŠčĆą░č鹊čĆč¢čŚ čĆč¢ąĘąĮąĖčģ ą║čĆą░茹Į ą░ą║čéąĖą▓ąĮąŠ ą┤ąŠčüą╗č¢ą┤ąČčāčÄčéčī čåč¢ čüą┐ąŠą╗čāą║ąĖ.
ąóą░ą║ąŠąČ, čāą▓ą░ą│čā ą┤ąŠčüą╗č¢ą┤ąĮąĖą║č¢ą▓ ą┐čĆąĖą▓ąĄčĆąĮčāą╗ąĖ ą┐čĆąĖčĆąŠą┤ąĮč¢ ą║ą░čéą░ą╗č¢ąĘą░č鹊čĆąĖ – č乥čĆą╝ąĄąĮčéąĖ – ąŠą║čüąĖą┤ąŠčĆąĄą┤čāą║čéą░ąĘąĖ, čÅą║č¢ ą║ą░čéą░ą╗č¢ąĘčāčÄčéčī ąŠą║ąĖčüąĮąŠ-ą▓č¢ą┤ąĮąŠą▓ąĮč¢ čĆąĄą░ą║čåč¢čŚ ą▓ ą▒č¢ąŠą╗ąŠą│č¢čćąĮąĖčģ čüąĖčüč鹥ą╝ą░čģ.
ążąĄčĆą╝ąĄąĮčéąĖ ąĘą░ ą▒čāą┤ąŠą▓ąŠčÄ č¢ čüą║ą╗ą░ą┤ąŠą╝ ŌĆō čåąĄ ą▒č¢ą╗ą║ąĖ. ąÆ ą╝ąŠą╗ąĄą║čāą╗ą░čģ č乥čĆą╝ąĄąĮčéč¢ą▓ ą┐čĆąŠčüčéąĖčģ ą▒č¢ą╗ą║č¢ą▓ čö čüą▓ąŠčöčĆč¢ą┤ąĮą░ ŌĆ£ą║ąĖčłąĄąĮčÅŌĆØ ą┐ąŠą╗č¢ą┐ąĄą┐čéąĖą┤ąĮąŠą│ąŠ ą╗ą░ąĮčåčÄą│ą░, ą▓ čÅą║č¢ą╣ č¢ ą▓č¢ą┤ą▒čāą▓ą░čÄčéčīčüčÅ ą║ą░čéą░ą╗č¢čéąĖčćąĮč¢ ą┐ąĄčĆąĄčéą▓ąŠčĆąĄąĮąĮčÅ čüčāą▒čüčéčĆą░čéčā.
ąæč¢ą╗čīčłč¢čüčéčī č乥čĆą╝ąĄąĮčéč¢ą▓ – čüą║ą╗ą░ą┤ąĮč¢ ą▒č¢ą╗ą║ąĖ (ą┐čĆąŠč鹥茹┤ąĖ). ąÆ čüą║ą╗ą░ą┤ąĮąĖčģ č乥čĆą╝ąĄąĮčéą░čģ ą▒č¢ą╗ą║ąŠą▓ąĖą╣ ą║ąŠą╝ą┐ąŠąĮąĄąĮčé ąĮą░ąĘąĖą▓ą░čÄčéčī ą░ą┐ąŠč乥čĆą╝ąĄąĮčé, ąĮąĄą▒č¢ą╗ą║ąŠą▓ąĖą╣ – ą║ąŠčäą░ą║č鹊čĆ. ąÜąŠčäą░ą║č鹊čĆąĖ ą┐ąŠą┤č¢ą╗čÅčÄčéčī ąĮą░: ą║ąŠč乥čĆą╝ąĄąĮčéąĖ, ą░ą║čéąĖą▓ą░č鹊čĆąĖ č¢ ą┐čĆąŠčüč鹥čéąĖčćąĮč¢ ą│čĆčāą┐ąĖ.
ąØąĄą▒č¢ą╗ą║ąŠą▓ą░ čćą░čüčéąĖąĮą░ čüą║ą╗ą░ą┤ąĮąŠą│ąŠ č乥čĆą╝ąĄąĮčéčā ą╝ąŠąČąĄ ą▒čāčéąĖ ąĘą▓ŌĆÖčÅąĘą░ąĮą░ ąĘ ą▒č¢ą╗ą║ąŠą▓ąŠčÄ (ą░ą┐ąŠč乥čĆą╝ąĄąĮč鹊ą╝) ąĮąĄ ąĄą║ą▓č¢ą▓ą░ą╗ąĄąĮčéąĮąĖą╝ čģč¢ą╝č¢čćąĮąĖą╝ ąĘą▓ŌĆÖčÅąĘą║ąŠą╝ (ą│č¢ą┤čĆąŠą│ąĄąĮąĮąĖą╣ ąĘą▓ŌĆÖčÅąĘąŠą║, ą│č¢ą┤čĆąŠčäč¢ą╗čīąĮą░ ą░ą▒ąŠ ą│č¢ą┤čĆąŠč乊ą▒ąĮą░ ą▓ąĘą░čöą╝ąŠą┤č¢čÅ). ąÆ čåčīąŠą╝čā ą▓ąĖą┐ą░ą┤ą║čā ąĮąĄą▒č¢ą╗ą║ąŠą▓čā čćą░čüčéąĖąĮčā č乥čĆą╝ąĄąĮčéčā ąĮą░ąĘąĖą▓ą░čÄčéčī ą║ąŠč乥čĆą╝ąĄąĮčé. ąÜąŠč乥čĆą╝ąĄąĮčéąĖ ąĘą┤ą░čéąĮč¢ ą╗ąĄą│ą║ąŠ ą▓č¢ą┤čēąĄą┐ą╗čÄą▓ą░čéąĖčüčÅ ą▓č¢ą┤ ą▒č¢ą╗ą║ąŠą▓ąŠčŚ čćą░čüčéąĖąĮąĖ č乥čĆą╝ąĄąĮčéčā.
ą¤čĆąŠčüč鹥čéąĖčćąĮč¢ ą│čĆčāą┐ąĖ ąĘą▓ŌĆÖčÅąĘą░ąĮč¢ ąĘ ą▒č¢ą╗ą║ąŠą▓ąŠčÄ čćą░čüčéąĖąĮąŠčÄ čüą║ą╗ą░ą┤ąĮąŠą│ąŠ č乥čĆą╝ąĄąĮčéčā ą║ąŠą▓ą░ą╗ąĄąĮčéąĮąĖą╝ ąĘą▓ŌĆÖčÅąĘą║ąŠą╝, čÅą║ąĖą╣ ą▓ą░ąČą║ąŠ čĆąŠąĘč¢čĆą▓ą░čéąĖ.
ąÉą║čéąĖą▓ą░č鹊čĆąĖ čåąĄ čéą░ą║č¢ ą║ąŠčäą░ą║č鹊čĆąĖ č乥čĆą╝ąĄąĮčéč¢ą▓, čēąŠ ą┐ąĄčĆąĄą▓ąŠą┤čÅčéčī ą╣ąŠą│ąŠ ą▓ ą░ą║čéąĖą▓ąĮąĖą╣ čüčéą░ąĮ, ą░ čüą░ą╝č¢ ą┐čĆąĖ čåčīąŠą╝čā ąĮąĄ ą▒ąĄčĆčāčéčī čāčćą░čüčéčī ą▓ ą║ą░čéą░ą╗č¢čéąĖčćąĮč¢ą╣ čĆąĄą░ą║čåč¢čŚ, ą┤ąŠ ąĮąĖčģ ą▓č¢ą┤ąĮąŠčüčÅčéčīčüčÅ ą▒ą░ą│ą░č鹊 ąĮąĄąŠčĆą│ą░ąĮč¢čćąĮąĖčģ č¢ąŠąĮč¢ą▓, ąĮą░ą┐čĆąĖą║ą╗ą░ą┤ č¢ąŠąĮąĖ ą╝ąĄčéą░ą╗č¢ą▓ ą╝ąĄčéą░ą╗č¢ą▓. ąÆ ą▒ą░ą│ą░čéčīąŠčģ čüą║ą╗ą░ą┤ąĮąĖčģ č乥čĆą╝ąĄąĮčéą░čģ, ą░ą║čéąĖą▓ąĮąĖą╝ čåąĄąĮčéčĆąŠą╝ čö ą╝ąĄčéą░ą╗ąŠą┐ąŠčĆčäč¢čĆąĖąĮąĖ.
ąóą░ą║, čā 80-čģ čĆąŠą║ą░čģ ą┐čĆąŠą▓ąĄą╗ąĖ čāčüą┐č¢čłąĮąĖą╣ ąĄą║čüą┐ąĄčĆąĖą╝ąĄąĮčé ąĘ ą▓ąĖą║ąŠčĆąĖčüčéą░ąĮąĮčÅą╝ č乥čĆą╝ąĄąĮčéčā ą╗ą░ą║čéą░ąĘą░. ążąĄčĆą╝ąĄąĮčé ą╗ą░ą║čéą░ąĘą░, č¢ą╝ąŠą▒č¢ą╗č¢ąĘąŠą▓ą░ąĮąĖą╣ (čłčéčāčćąĮąŠ ą┐čĆąĖą▓ŌĆÖčÅąĘą░ąĮąĖą╣ ą┤ąŠ čüčāą▒čüčéčĆą░čéčā) ąĮą░ ąĄą╗ąĄą║čéčĆąŠą┤č¢ ąĘ čüą░ąČč¢, ą▓č¢ą┤ąĮąŠą▓ą╗čÄą▓ą░ą▓ ą║ąĖčüąĄąĮčī. ąĪąĖą╗ą░ čüčéčĆčāą╝čā, čÅą║ąĖą╣ ąŠčéčĆąĖą╝ą░ą╗ąĖ ą┤ąŠčüą╗č¢ą┤ąĮąĖą║ąĖ ą▒čāą╗ą░ ąĮąĄą▓ąĄą╗ąĖą║ą░, ą░ą╗ąĄ čüąĖčüč鹥ą╝ą░ ą┐čĆąŠą┐čĆą░čåčÄą▓ą░ą╗ą░ 50 ą│ąŠą┤ąĖąĮ.
ą¦ąĖčüą╗ąĄąĮąĮč¢ ąĄą║čüą┐ąĄčĆąĖą╝ąĄąĮčéąĖ č¢ ą┤ąŠčüą╗č¢ą┤ąČąĄąĮąĮčÅ ą┐čĆąĖąĘą▓ąĄą╗ąĖ ą┤ąŠ čüčéą▓ąŠčĆąĄąĮąĮčÅ ą║č¢ą╗čīą║ąŠčģ čéąĖą┐č¢ą▓ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓.
ąóąĖą┐ąĖ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓
ą¤ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé ąĘ ą╝ąĄą╝ą▒čĆą░ąĮąŠčÄ ąŠą▒ą╝č¢ąĮčā ą┐čĆąŠč鹊ąĮč¢ą▓.
ą¤ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé ąĘ ą┐čĆąŠč鹊ąĮąŠąŠą▒ą╝č¢ąĮąĮąŠčÄ ą╝ąĄą╝ą▒čĆą░ąĮąŠčÄ ą▓ąĖą║ąŠčĆąĖčüč鹊ą▓čāčö ą┐ąŠą╗č¢ą╝ąĄčĆąĮąĖą╣ ąĄą╗ąĄą║čéčĆąŠą╗č¢čé. ą”ąĄą╣ čéąĖą┐ ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéčā čö ąŠą┤ąĮč¢čöčÄ ąĘ ąĮą░ą╣ą▒č¢ą╗čīčł čĆąŠąĘą▓ąĖąĮąĄąĮąĖčģ č¢ čćą░čüč鹊 ą▓ąĖą║ąŠčĆąĖčüč鹊ą▓čāą▓ą░ąĮąĖčģ čüąĖčüč鹥ą╝ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓; ąŠą▒ą╗ą░čüčéč¢ ą╣ąŠą│ąŠ ąĘą░čüč鹊čüčāą▓ą░ąĮąĮčÅ ą┐ąŠčłąĖčĆčÄčÄčéčīčüčÅ ąĮą░ čéčĆą░ąĮčüą┐ąŠčĆčé, ą┐ąŠčĆčéą░čéąĖą▓ąĮč¢ ą┤ąČąĄčĆąĄą╗ą░ ąČąĖą▓ą╗ąĄąĮąĮčÅ č¢ ą┐čĆąĖčüčéčĆąŠčŚ ąĘą░ą▒ąĄąĘą┐ąĄč湥ąĮąĮčÅ čĆąĄąĘąĄčĆą▓ąĮąŠą│ąŠ ąČąĖą▓ą╗ąĄąĮąĮčÅ. ą¤ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé ąĘ ą╝ąĄą╝ą▒čĆą░ąĮąŠčÄ ąŠą▒ą╝č¢ąĮčā ą┐čĆąŠč鹊ąĮč¢ą▓ ą╝ą░čö ą║ąŠą╝ą┐ą░ą║čéąĮčā ą║ąŠąĮčüčéčĆčāą║čåč¢čÄ č¢ ąĘą░ą▒ąĄąĘą┐ąĄčćčāčö ą▓ąĖčüąŠą║čā ąĄč乥ą║čéąĖą▓ąĮč¢čüčéčī ą┤ąŠ ą╝ą░čüąĖ. ą®ąĄ ąŠą┤ąĮč¢čöčÄ ą┐ąĄčĆąĄą▓ą░ą│ąŠčÄ čö ą╝ąŠąČą╗ąĖą▓č¢čüčéčī čłą▓ąĖą┤ą║ąŠą│ąŠ ąĘą░ą┐čāčüą║čā ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéčā ą▓ čĆąŠą▒ąŠčéčā. ą¤ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé ą┐čĆą░čåčÄčö ą┐čĆąĖ č鹥ą╝ą┐ąĄčĆą░čéčāčĆč¢ ą▓ 80*ąĪ, ą╣ąŠą│ąŠ ąÜąÜąö čüčéą░ąĮąŠą▓ąĖčéčī 50%.
ąöąŠ ąĮąĄą┤ąŠą╗č¢ą║č¢ą▓ čüąĖčüč鹥ą╝ ąĘ ą┐čĆąŠč鹊ąĮąŠąŠą▒ą╝č¢ąĮąĮąŠčÄ ą╝ąĄą╝ą▒čĆą░ąĮąŠčÄ ą╝ąŠąČąĮą░ ą▓č¢ą┤ąĮąĄčüčéąĖ ą▓ąĖčüąŠą║č¢ ą▓ąĖčĆąŠą▒ąĮąĖčćč¢ ą▓ąĖčéčĆą░čéąĖ čéą░ čüą║ą╗ą░ą┤ąĮčā čüąĖčüč鹥ą╝čā čāą┐čĆą░ą▓ą╗č¢ąĮąĮčÅ čĆąŠą▒ąŠč鹊čÄ ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéčā. ą»ą┤čĆąŠ ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéčā ąĮąĄ ą╝ąŠąČąĄ ą▒čāčéąĖ ąĘą░ą┐čāčēąĄąĮąŠ ą┐čĆąŠčüčéąĖą╝ ą┐čĆąŠą┤čāą▓ą░ąĮąĮčÅą╝ ą▓ąŠą┤ąĮčÄ č¢ ą║ąĖčüąĮčÄ, ąĮąĄąŠą▒čģč¢ą┤ąĮą░ ą┐ąĄą▓ąĮą░ čüčéą░čĆč鹊ą▓ą░ ą║č¢ą╗čīą║č¢čüčéčī ą▓ąŠą┤ąĖ ą▓ ąĮčīąŠą╝čā. ą¤ą░ą╗ąĖą▓ąŠ ą┤ą╗čÅ ąĄą╗ąĄą╝ąĄąĮčéą░, ą▓ąŠą┤ąĄąĮčī, ą┐ąŠą▓ąĖąĮąĄąĮ ą▒čāčéąĖ ąĮą░ą┤ąĘą▓ąĖčćą░ą╣ąĮąŠ ąŠčćąĖčēąĄąĮąĖą╝, č¢ąĮą░ą║čłąĄ ą┐čĆąŠč鹊ąĮąŠąŠą▒ą╝č¢ąĮąĮą░ ą╝ąĄą╝ą▒čĆą░ąĮą░ čłą▓ąĖą┤ą║ąŠ ą┐čüčāčöčéčīčüčÅ. ąØą░ą╗ą░ą│ąŠą┤ąČąĄąĮąĮčÅ čéą░ ąŠą▒čüą╗čāą│ąŠą▓čāą▓ą░ąĮąĮčÅ čüąĖčüč鹥ą╝ čéą░ą║ąĖčģ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓ ą▓ą║čĆą░ą╣ čüą║ą╗ą░ą┤ąĮč¢; ąĮą░ą┐čĆąĖą║ą╗ą░ą┤, 150-ą▓ąŠą╗čīč鹊ą▓ą░ ą▒ą░čéą░čĆąĄčÅ ąĮą░ą╗č¢čćčāčö 250 ąŠą║čĆąĄą╝ąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓, čÅą║č¢ ąĮąĄąŠą▒čģč¢ą┤ąĮąŠ ą┐čĆą░ą▓ąĖą╗čīąĮąŠ ąĮą░ą╗ą░čłčéčāą▓ą░čéąĖ.
ą¤ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé čćčāčéą╗ąĖą▓ąĖą╣ ą┤ąŠ ąĮąĖąĘčīą║ąĖčģ č鹥ą╝ą┐ąĄčĆą░čéčāčĆ, ą░ą┤ąČąĄ čåąĄ ą╝ąŠąČąĄ ą┐čĆąĖąĘą▓ąĄčüčéąĖ ą┤ąŠ čāčéą▓ąŠčĆąĄąĮąĮčÅ ą╗čīąŠą┤čā. ą”ąĄ ąĘą╝čāčłčāčö ą┤ąŠą┤ą░ą▓ą░čéąĖ ą▓ ą║ąŠąĮčüčéčĆčāą║čåč¢čÄ ąĮą░ą│čĆč¢ą▓ą░ą╗čīąĮč¢ ąĄą╗ąĄą╝ąĄąĮčéąĖ, čÅą║č¢ ąĘą▒č¢ą╗čīčłčāčÄčéčī ą║č¢ąĮčåąĄą▓čā ą▓ą░čĆčéč¢čüčéčī ą┐čĆąĖčüčéčĆąŠčÄ. ąŚą░ą┐čāčüą║ ą▓ čģąŠą╗ąŠą┤ąĮčā ą┐ąŠą│ąŠą┤čā ą╝ąŠąČąĄ čéčĆąĖą▓ą░čéąĖ ą┤ąŠą▓čłąĄ, ą░ ą┐čĆąŠą┤čāą║čéąĖą▓ąĮč¢čüčéčī ą┐ąŠą╝č¢čéąĮąŠ ąĮąĖąČč湥. ąØą░ą┤ą╝č¢čĆąĮąĄ č鹥ą┐ą╗ąŠčāčéą▓ąŠčĆąĄąĮąĮčÅ čéą░ą║ąŠąČ ą╝ąŠąČąĄ ą┐čĆąĖąĘą▓ąĄčüčéąĖ ą┤ąŠ ą┐ąŠčłą║ąŠą┤ąČąĄąĮąĮčÅ ą┐ą░ą╗ąĖą▓ąĮąŠčŚ ą║ąŠą╝č¢čĆą║ąĖ. ąĪąĖčüč鹥ą╝ąĖ ą║ąŠąĮčéčĆąŠą╗čÄ č鹥ą╝ą┐ąĄčĆą░čéčāčĆąĖ č¢ ą┐ąŠą┤ą░čćč¢ ą║ąĖčüąĮčÄ čüą┐ąŠąČąĖą▓ą░čÄčéčī ą▒ą╗ąĖąĘčīą║ąŠ 30% ąĄą╗ąĄą║čéčĆąŠąĄąĮąĄčĆą│č¢čŚ, čÅą║čā ą│ąĄąĮąĄčĆčāčö ą┐ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé.
ą¤čĆąĖ ą▓čüčéą░ąĮąŠą▓ą╗ąĄąĮąĮč¢ ą▓ čéčĆą░ąĮčüą┐ąŠčĆčéąĮąĖą╣ ąĘą░čüč¢ą▒, ą┐ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé ąĘ ą┐čĆąŠč鹊ąĮąŠąŠą▒ą╝č¢ąĮąĮąŠčÄ ą╝ąĄą╝ą▒čĆą░ąĮąŠčÄ ą╝ą░čö čĆąŠąĘčĆą░čģčāąĮą║ąŠą▓ąĖą╣ č鹥čĆą╝č¢ąĮ čüą╗čāąČą▒ąĖ 2000-4000 ą│ąŠą┤ąĖąĮ. ąÆąĮą░čüą╗č¢ą┤ąŠą║ ąĮąĄčĆč¢ą▓ąĮąŠą╝č¢čĆąĮąŠą│ąŠ ąĮą░ą▓ą░ąĮčéą░ąČąĄąĮąĮčÅ ą▓č¢ą┤ą▒čāą▓ą░čöčéčīčüčÅ ąĘą░ą╣ą▓ąĄ ąĘą▓ąŠą╗ąŠąČąĄąĮąĮčÅ ą░ą▒ąŠ, ąĮą░ą▓ą┐ą░ą║ąĖ, ą▓ąĖčüąĖčģą░ąĮąĮčÅ ą┐ą░ą╗ąĖą▓ąĮąŠčŚ ą║ąŠą╝č¢čĆą║ąĖ, čēąŠ čüą┐čĆąĖčÅčö ąĘąĮąŠčüčā ą╝ąĄą╝ą▒čĆą░ąĮąĖ. ą¤čĆąĖ čāčüčéą░ąĮąŠą▓čåč¢ ą▓ ą┐čĆąĖčüčéčĆč¢ą╣ ąĘ ą▒ąĄąĘą┐ąĄčĆąĄčĆą▓ąĮąĖą╝ čåąĖą║ą╗ąŠą╝ čĆąŠą▒ąŠčéąĖ, ą┐ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé ąĘą┤ą░čéąĮąĖą╣ ąĮąŠčĆą╝ą░ą╗čīąĮąŠ čäčāąĮą║čåč¢ąŠąĮčāą▓ą░čéąĖ ą┐čĆąŠčéčÅą│ąŠą╝ 40000 ą│ąŠą┤ąĖąĮ. ąŚąĮąĖąČąĄąĮąĮčÅ čäčāąĮą║čåč¢ąŠąĮą░ą╗čīąĮąŠčüčéč¢ ą▓č¢ą┤ą▒čāą▓ą░čöčéčīčüčÅ ą┐ą╗ą░ą▓ąĮąŠ, čēąŠ čĆąŠą▒ąĖčéčī ą╣ąŠą│ąŠ čüčģąŠąČąĖą╝ ąĮą░ ąĄą╗ąĄą║čéčĆąŠčģč¢ą╝č¢čćąĮčā ą▒ą░čéą░čĆąĄčÄ. ąŚą░ą╝č¢ąĮą░ čÅą┤čĆą░ (čüč鹥ą║ą░) ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéą░ čö ąŠčüąĮąŠą▓ąĮąŠčÄ ą▓ąĖčéčĆą░čéąĮąŠčÄ čćą░čüčéąĖąĮąŠčÄ ąŠą▒čüą╗čāą│ąŠą▓čāą▓ą░ąĮąĮčÅ.
ąøčāąČąĮąĖą╣ ą┐ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé.
ąøčāąČąĮč¢ ą┐ą░ą╗ąĖą▓ąĮč¢ ąĄą╗ąĄą╝ąĄąĮčéąĖ ąŠčéčĆąĖą╝ą░ą╗ąĖ ąĮą░ą╣ą▒č¢ą╗čīčłąĄ ąĘą░čüč鹊čüčāą▓ą░ąĮąĮčÅ ą▓ ą║ąŠčüą╝č¢čćąĮč¢ą╣ ą│ą░ą╗čāąĘč¢ (ą▓ č鹊ą╝čā čćąĖčüą╗č¢, ą┤ą╗čÅ ą║ąŠčüą╝č¢čćąĮąĖčģ ą║ąŠčĆą░ą▒ą╗č¢ą▓ ą▒ą░ą│ą░č鹊čĆą░ąĘąŠą▓ąŠą│ąŠ ą▓ąĖą║ąŠčĆąĖčüčéą░ąĮąĮčÅ). ąÆą░čĆčéč¢čüčéčī ą▓ąĖčĆąŠą▒ąĮąĖčåčéą▓ą░ č¢ ąŠą▒čüą╗čāą│ąŠą▓čāą▓ą░ąĮąĮčÅ, ąŠčüąŠą▒ą╗ąĖą▓ąŠ ą┤ą╗čÅ čÅą┤čĆą░ ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéą░, čö ą┐ąŠčĆč¢ą▓ąĮčÅąĮąŠ ą┤ąŠčüčéčāą┐ąĮąĖą╝ąĖ. ąØą░ą┐čĆąĖą║ą╗ą░ą┤, čüąĄą┐ą░čĆą░č鹊čĆ ą┤ą╗čÅ ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéą░ ąĘ ą┐čĆąŠč鹊ąĮąŠąŠą▒ą╝č¢ąĮąĮąŠčÄ ą╝ąĄą╝ą▒čĆą░ąĮąŠčÄ ą║ąŠčłčéčāčö ą▓č¢ą┤ $800 ą┤ąŠ $1100 ąĘą░ ą║ą▓ą░ą┤čĆą░čéąĮąĖą╣ ą╝ąĄčéčĆ, ą░ ą┤ą╗čÅ ą╗čāąČąĮąŠą│ąŠ ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéčā ą╣ąŠą│ąŠ ą▓ą░čĆčéč¢čüčéčī ąĮą░ą▓č¢čéčī ąĮąĄ ą▒ąĄčĆąĄčéčīčüčÅ ą▓ čĆąŠąĘčĆą░čģčāąĮąŠą║ (ą▓ąŠąĮą░ čüčéą░ąĮąŠą▓ąĖčéčī $5). ąÜąŠąĄčäč¢čåč¢čöąĮčé ą║ąŠčĆąĖčüąĮąŠčŚ ą┤č¢čŚ čéą░ą║ąŠą│ąŠ ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéą░ ąĘąĮą░čģąŠą┤ąĖčéčīčüčÅ ą▓ čĆą░ą╣ąŠąĮč¢ 60%. ąÉą╗ąĄ čā ąĮčīąŠą│ąŠ čö č¢ ąĮąĄą┤ąŠą╗č¢ą║ąĖ, ąĮą░ą┐čĆąĖą║ą╗ą░ą┤, ą╣ąŠą│ąŠ čäč¢ąĘąĖčćąĮč¢ čĆąŠąĘą╝č¢čĆąĖ ą║ąŠąĮčüčéčĆčāą║čéąĖą▓ąĮąŠ ą▒č¢ą╗čīčłąĄ, ąĮč¢ąČ čā ą▓ąĄčĆčüč¢čŚ ąĘ ą┐čĆąŠč鹊ąĮąŠąŠą▒ą╝č¢ąĮąĮąŠčÄ ą╝ąĄą╝ą▒čĆą░ąĮąŠčÄ, čéą░ą║ąŠąČ ą╣ąŠą╝čā ąĮąĄąŠą▒čģč¢ą┤ąĮąĖą╣ ą▓ą║čĆą░ą╣ čćąĖčüčéąĖą╣ ą▓ąŠą┤ąĄąĮčī č¢ ą║ąĖčüąĄąĮčī. ąÆąĖą║ąŠčĆąĖčüčéą░ąĮąĮčÅ ą║ąĖčüąĮčÄ ąĘ ąĮą░ą▓ą║ąŠą╗ąĖčłąĮčīąŠą│ąŠ čüąĄčĆąĄą┤ąŠą▓ąĖčēą░, ą▓ čüą║ą╗ą░ą┤č¢ čÅą║ąŠą│ąŠ čö ą║ą░čĆą▒ąŠąĮ ą┤ąĖąŠą║čüąĖą┤, ą╝ąŠąČąĄ ą▓ąĖą▓ąĄčüčéąĖ čéą░ą║ąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé ąĘ ą╗ą░ą┤čā. ąöą░ąĮč¢ ąĮąĄą┤ąŠą╗č¢ą║ąĖ ąŠą▒ą╝ąĄąČčāčÄčéčī ąĘą░čüč鹊čüčāą▓ą░ąĮąĮčÅ ą╗čāąČąĮąĖčģ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓.
ąóą▓ąĄčĆą┤ąŠąŠą║čüąĖą┤ąĮąĖą╣ ą┐ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé.
ąóą▓ąĄčĆą┤ąŠąŠą║čüąĖą┤ąĮąĖą╣ ą┐ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé čö ąĮą░ą╣ą╝ąĄąĮčł ą┐ąŠčłąĖčĆąĄąĮąĖą╝, ą░ą╗ąĄ ąŠčüčéą░ąĮąĮč¢ą╝ čćą░čüąŠą╝ č湥čĆąĄąĘ ą┐čĆąŠčĆąĖą▓ ą▓ ą┤ąŠčüą╗č¢ą┤ąČąĄąĮąĮčÅčģ ą╝ą░č鹥čĆč¢ą░ą╗č¢ą▓ č¢ čāčüčéą░čéą║čāą▓ą░ąĮąĮčÅ čÅą┤čĆą░ ąĄą╗ąĄą╝ąĄąĮčéą░, ąĮą░ čåčÄ č鹥čģąĮąŠą╗ąŠą│č¢čÄ ąĘą▓ąĄčĆąĮčāą╗ąĖ čāą▓ą░ą│čā. ąŚą░ą▓ą┤čÅą║ąĖ ąĮąŠą▓ąŠą╝čā ą┐ąŠą║ąŠą╗č¢ąĮąĮčÄ ą║ąĄčĆą░ą╝č¢čćąĮąĖčģ ą╝ą░č鹥čĆč¢ą░ą╗č¢ą▓ ą▓ą┤ą░ą╗ąŠčüčÅ ąĘąĮąĖąĘąĖčéąĖ čĆąŠą▒ąŠčćčā č鹥ą╝ą┐ąĄčĆą░čéčāčĆčā ąĘ 800-1000*ąĪ ą┤ąŠ 500-600*ąĪ.
ąÆąĖčüąŠą║ą░ č鹥ą╝ą┐ąĄčĆą░čéčāčĆą░ ą┤ąŠąĘą▓ąŠą╗čÅčö ąĘą┤č¢ą╣čüąĮčÄą▓ą░čéąĖ ąŠą║ąĖčüąĮąĄąĮąĮčÅ ą┐čĆąĖčĆąŠą┤ąĮąŠą│ąŠ ą│ą░ąĘčā ąĘą░ ą┤ąŠą┐ąŠą╝ąŠą│ąŠčÄ ą┐čĆąŠčåąĄčüčā ą║ą░čéą░ą╗č¢čéąĖčćąĮąŠą│ąŠ čĆąĖč乊čĆą╝č¢ąĮą│čā. ąĪą░ą╝ąĄ ąĘą┤ą░čéąĮč¢čüčéčī čüą┐ąŠąČąĖą▓ą░čéąĖ ą║ą░čĆą▒ąŠą│č¢ą┤čĆąŠą│ąĄąĮąĮąĄ ą┐ą░ą╗ąĖą▓ąŠ ą▒ąĄąĘ ąĮąĄąŠą▒čģč¢ą┤ąĮąŠčüčéč¢ ą┐ąŠą┐ąĄčĆąĄą┤ąĮčīąŠą│ąŠ čĆąĖč乊čĆą╝č¢ąĮą│čā ąĘą░ą▒ąĄąĘą┐ąĄčćčāčö ą▓ąĖčüąŠą║čā ąĄč乥ą║čéąĖą▓ąĮč¢čüčéčī č¢ čüčéą▓ąŠčĆčÄčö ąĘąĮą░čćąĮč¢ ą┐ąĄčĆąĄą▓ą░ą│ąĖ ą┤ą╗čÅ čåčīąŠą│ąŠ čéąĖą┐čā ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓. ą¤ąŠą▒č¢čćąĮąĖą╝ ą┐čĆąŠą┤čāą║č鹊ą╝ čĆąŠą▒ąŠčéąĖ čéą▓ąĄčĆą┤ąŠąŠą║čüąĖą┤ąĮąŠą│ąŠ ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéčā čö č鹥ą┐ą╗ąŠčāčéą▓ąŠčĆąĄąĮąĮčÅ, čÅą║ąĄ ą╝ąŠąČąĮą░ ą▓ąĖą║ąŠčĆąĖčüč鹊ą▓čāą▓ą░čéąĖ ą┤ą╗čÅ ą│ąĄąĮąĄčĆą░čåč¢čŚ ąĄą╗ąĄą║čéčĆąĖą║ąĖ ąĘą░ ą┤ąŠą┐ąŠą╝ąŠą│ąŠčÄ čéčāčĆą▒č¢ąĮ, ąÜąÜąö čéą▓ąĄčĆą┤ąŠąŠą║čüąĖą┤ąĮąĖčģ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓ ą╝ąŠąČąĄ ą┤ąŠčüčÅą│ą░čéąĖ 90%, čēąŠ čö ąĮą░ą╣ą▓ąĖčēąĖą╝ ą┐ąŠą║ą░ąĘąĮąĖą║ąŠą╝ čüąĄčĆąĄą┤ ą▓čüč¢čģ ą▓ąĖą┤č¢ą▓ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓. ąĪąĄčĆąĄą┤ ąĮąĄą┤ąŠą╗č¢ą║č¢ą▓ – ąĮąĄąŠą▒čģč¢ą┤ąĮč¢čüčéčī ą▓ąĖą║ąŠčĆąĖčüčéą░ąĮąĮčÅ č鹥čĆą╝ąŠčüčéč¢ą╣ą║ąĖčģ č¢ ą┤ąŠčĆąŠą│ąĖčģ ą╝ą░č鹥čĆč¢ą░ą╗č¢ą▓ ą┤ą╗čÅ čÅą┤čĆą░ ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéą░, čÅą║č¢ ą╝ą░čÄčéčī ąŠą▒ą╝ąĄąČąĄąĮąĖą╣ č鹥čĆą╝č¢ąĮ čüą╗čāąČą▒ąĖ.
ą¤ą░ą╗ąĖą▓ąĮąĖą╣ ąĄą╗ąĄą╝ąĄąĮčé ąĘ ą┐čĆčÅą╝ąĖą╝ ąŠą║ąĖčüąĮąĄąĮąĮčÅą╝ ą╝ąĄčéą░ąĮąŠą╗čā.
ą¤ąŠčĆčéą░čéąĖą▓ąĮč¢ ą┐ą░ą╗ąĖą▓ąĮč¢ ąĄą╗ąĄą╝ąĄąĮčéąĖ čö ą▓ą║čĆą░ą╣ čåč¢ą║ą░ą▓ąĖą╝ąĖ ą┤ą╗čÅ čĆąŠąĘčĆąŠą▒ąĮąĖą║č¢ą▓ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓, č¢ ąĮą░ą╣ą▒č¢ą╗čīčł ą┐ąĄčĆčüą┐ąĄą║čéąĖą▓ąĮą░ č鹥čģąĮąŠą╗ąŠą│č¢čÅ ą┤ą╗čÅ čŚčģ čüčéą▓ąŠčĆąĄąĮąĮčÅ – čåąĄ ą┐čĆčÅą╝ąĄ ąŠą║ąĖčüąĮąĄąĮąĮčÅ ą╝ąĄčéą░ąĮąŠą╗čā. ą¤ą░ą╗ąĖą▓ąĮč¢ ąĄą╗ąĄą╝ąĄąĮčéąĖ ąĘ ą┐čĆčÅą╝ąĖą╝ ąŠą║ąĖčüą╗ąĄąĮąĮčÅą╝ ą╝ąĄčéą░ąĮąŠą╗čā ą╝ą░čÄčéčī ąĮąĄą▓ąĄą╗ąĖą║ąĖą╣ čĆąŠąĘą╝č¢čĆ, ąĮąĄą┤ąŠčĆąŠą│č¢ čā ą▓ąĖą│ąŠč鹊ą▓ą╗ąĄąĮąĮč¢, ąĘčĆčāčćąĮč¢ čā ą▓ąĖą║ąŠčĆąĖčüčéą░ąĮąĮč¢ č¢ ąĮąĄ ą▓ąĖą╝ą░ą│ą░čÄčéčī čüčéąĖčüąĮąĄąĮąŠą│ąŠ ą│ą░ąĘąŠą┐ąŠą┤č¢ą▒ąĮąŠą│ąŠ ą▓ąŠą┤ąĮčÄ. ą¤ą░ą╗ąĖą▓ąĮč¢ ąĄą╗ąĄą╝ąĄąĮčéąĖ ą┐čĆčÅą╝ąŠą│ąŠ ąŠą║ąĖčüąĮąĄąĮąĮčÅ ą╝ąĄčéą░ąĮąŠą╗čā ą╝ą░čÄčéčī ą│ą░čĆąĮč¢ ąĄą╗ąĄą║čéčĆąŠčģč¢ą╝č¢čćąĮč¢ čģą░čĆą░ą║č鹥čĆąĖčüčéąĖą║ąĖ, čŚčģ ąĘą░ą┐čĆą░ą▓ą║ą░ ą┐čĆąŠą▓ąŠą┤ąĖčéčīčüčÅ čłą╗čÅčģąŠą╝ čāą┐čĆąĖčüą║čāą▓ą░ąĮąĮčÅ čĆč¢ą┤ąĖąĮąĖ ą░ą▒ąŠ ąĘą░ą╝č¢ąĮąĖ ą║ą░čĆčéčĆąĖą┤ąČą░, čēąŠ ą┤ąŠąĘą▓ąŠą╗čÅčö ą┐čĆąŠą┤ąŠą▓ąČčāą▓ą░čéąĖ čĆąŠą▒ąŠčéčā ą▒ąĄąĘ ą┐čĆąŠčüč鹊茹▓.
ąŚą░ą│ą░ą╗ąŠą╝, čüčāčćą░čüąĮąĖą╝ ą┐ą░ą╗ąĖą▓ąĮąĖą╝ ąĄą╗ąĄą╝ąĄąĮčéą░ą╝ ą┐čĆąĖčéą░ą╝ą░ąĮąĮč¢ čéą░ą║č¢ ąŠą▒ą╝ąĄąČąĄąĮąĮčÅ čÅą║ ą┐ąŠą▓č¢ą╗čīąĮąĖą╣ ąĘą░ą┐čāčüą║, ąĮąĖąĘčīą║ą░ ą▓ąĖčģč¢ą┤ąĮą░ ą┐ąŠčéčāąČąĮč¢čüčéčī, ą┐ąŠą▓č¢ą╗čīąĮą░ čĆąĄą░ą║čåč¢čÅ ąĮą░ ą┐ąŠčéčĆąĄą▒čā ą▓ ąĄą╗ąĄą║čéčĆąŠąĄąĮąĄčĆą│č¢čŚ, ą┐ąŠą│ą░ąĮč¢ čģą░čĆą░ą║č鹥čĆąĖčüčéąĖą║ąĖ ąĮą░ą▓ą░ąĮčéą░ąČąĄąĮčī, ąĮąĖąĘčīą║ąĖą╣ ą┤č¢ą░ą┐ą░ąĘąŠąĮ ą┐ąŠčéčāąČąĮąŠčüčéč¢, ą║ąŠčĆąŠčéą║ąĖą╣ č鹥čĆą╝č¢ąĮ čüą╗čāąČą▒ąĖ č¢ ą▓ąĖčüąŠą║ą░ ą▓ą░čĆčéč¢čüčéčī. ą¤ąŠą┤č¢ą▒ąĮąŠ ąĄą╗ąĄą║čéčĆąĖčćąĮąĖą╝ ą▒ą░čéą░čĆąĄčÅą╝, ą┐čĆąŠą┤čāą║čéąĖą▓ąĮč¢čüčéčī ą▓čüč¢čģ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓ ąĘąĮąĖąČčāčöčéčīčüčÅ ąĘ ą▓č¢ą║ąŠą╝, čåąĄ ą▓č¢ą┤ą▒čāą▓ą░čöčéčīčüčÅ č湥čĆąĄąĘ ą┐ąŠčüčéčāą┐ąŠą▓čā ą┤ąĄą│čĆą░ą┤ą░čåč¢čÄ ą║ąŠą╝ą┐ąŠąĮąĄąĮčéč¢ą▓ čÅą┤čĆą░ (čüč鹥ą║ą░) ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéą░.
ą¤ą░ą╗ąĖą▓ąĮąĖą╝ ąĄą╗ąĄą╝ąĄąĮčéą░ą╝ ą┐ąŠčéčāąČąĮč¢čüčéčÄ ą╝ąĄąĮčłąĄ 1 ą║ąÆčé, čÅą║ ą┐čĆą░ą▓ąĖą╗ąŠ, ąĮąĄ ą┐ąŠčéčĆč¢ą▒ąĄąĮ čéąĖčüą║ ą┐čĆąĖ čĆąŠą▒ąŠčéč¢, č¢ ą┐ąŠą┤ą░čćą░ ą║ąĖčüąĮčÄ ą▓č¢ą┤ą▒čāą▓ą░čöčéčīčüčÅ čéč¢ą╗čīą║ąĖ ąĘą░ ą┤ąŠą┐ąŠą╝ąŠą│ąŠčÄ ą▓ąĄąĮčéąĖą╗čÅč鹊čĆą░; čüąĖčüč鹥ą╝ąĖ ąČąĖą▓ą╗ąĄąĮąĮčÅ ąĘ ą┐ąŠčéčāąČąĮč¢čüčéčÄ ą┐ąŠąĮą░ą┤ 1 ą║ąÆčé ą│ąĄčĆą╝ąĄčéąĖčćąĮč¢ čéą░ ąŠą▒ą╗ą░ą┤ąĮą░ąĮč¢ ą║ąŠą╝ą┐čĆąĄčüąŠčĆąŠą╝, čÅą║ąĖą╣ ąĘąĮąĖąČčāčö ąĘą░ą│ą░ą╗čīąĮčā ąĄč乥ą║čéąĖą▓ąĮč¢čüčéčī. ąÆč¢ą┤ąĮąŠčüąĮąŠ ą▓ąĖčüąŠą║ąĖą╣ ą▓ąĮčāčéčĆč¢čłąĮč¢ą╣ ąŠą┐č¢čĆ čÅą▓ą╗čÅčö čüąŠą▒ąŠčÄ čēąĄ ąŠą┤ąĮčā ą┐čĆąŠą▒ą╗ąĄą╝čā. ąÜąŠąČąĮą░ ą┐ą░ą╗ąĖą▓ąĮą░ ą║ąŠą╝č¢čĆą║ą░ čüč鹥ą║čā ą▓ąĖčĆąŠą▒ą╗čÅčö ą▒ą╗ąĖąĘčīą║ąŠ 1 ąÆ, ą┐č¢ą┤ą║ą╗čÄč湥ąĮąĮčÅ ą▓ąĄą╗ąĖą║ąŠą│ąŠ ąĮą░ą▓ą░ąĮčéą░ąČąĄąĮąĮčÅ ą┐čĆąĖąĘą▓ąŠą┤ąĖčéčī ą┤ąŠ ą┐ąŠą╝č¢čéąĮąŠą│ąŠ ą┐ą░ą┤č¢ąĮąĮčÅ ąĮą░ą┐čĆčāą│ąĖ. ą¤ąŠą┤č¢ą▒ąĮąŠ ąĄą╗ąĄą║čéčĆąĖčćąĮč¢ą╣ ą▒ą░čéą░čĆąĄčŚ, ą┐ąŠčéčāąČąĮč¢čüčéčī ą┐ą░ą╗ąĖą▓ąĮąŠą│ąŠ ąĄą╗ąĄą╝ąĄąĮčéą░ ąĘą╝ąĄąĮčłčāčöčéčīčüčÅ ąĘ ą▓č¢ą║ąŠą╝. ą×ą║čĆąĄą╝č¢ ą║ąŠą╝č¢čĆą║ąĖ ą╝ąŠąČčāčéčī ą▓ąĖčģąŠą┤ąĖčéąĖ ąĘ ą╗ą░ą┤čā č¢ ą▓ąĖą║ą╗ąĖą║ą░čéąĖ ąĘą▒ąŠčŚ ą▓ čĆąŠą▒ąŠčéč¢, čēąŠ ą┐čĆąĖąĘą▓ąŠą┤čÅčéčī ą┤ąŠ ąĮąĄą┐čĆą░ą▓ąĖą╗čīąĮąŠą│ąŠ čäčāąĮą║čåč¢ąŠąĮčāą▓ą░ąĮąĮčÅ ą▓čüč¢čöčŚ čüąĖčüč鹥ą╝ąĖ ą░ą▒ąŠ ąĘą░ą▒čĆčāą┤ąĮąĄąĮąĮčÅ ąĮą░ą▓ą║ąŠą╗ąĖčłąĮčīąŠą│ąŠ čüąĄčĆąĄą┤ąŠą▓ąĖčēą░.
ąöąŠčüą╗č¢ą┤ąČąĄąĮąĮčÅ ą▓ čüč乥čĆč¢ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓ ą┐čĆąŠą┤ąŠą▓ąČčāčÄčéčīčüčÅ č¢ ą┤ąŠ čüčīąŠą│ąŠą┤ąĮč¢. ąÆ ąĮą░čāą║ąŠą▓ąĖčģ ąĮąŠą▓ąĖąĮą░čģ ą╝ąŠąČąĮą░ ąĘčāčüčéčĆč¢čéąĖ čüčéą░čéčéč¢ ą┐čĆąŠ čĆąĄąĘčāą╗čīčéą░čéąĖ ą┤ąŠčüą╗č¢ą┤ąČąĄąĮčī č¢ ąĄą║čüą┐ąĄčĆąĖą╝ąĄąĮčéč¢ą▓, čÅą║č¢ čéą░ą║ čćąĖ č¢ąĮą░ą║čłąĄ čüč鹊čüčāčÄčéčīčüčÅ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓.
ąÆąČąĄ čüčéą▓ąŠčĆąĄąĮąŠ čüąĄčĆč¢ą╣ąĮč¢ ąĄą╗ąĄą║čéčĆąĖčćąĮč¢ ą░ą▓č鹊ą╝ąŠą▒č¢ą╗č¢ ąĮą░ ą▓ąŠą┤ąĮąĄą▓ąŠ-ą║ąĖčüąĮąĄą▓ąĖčģ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéą░čģ. ąÜąŠą╝ą┐ą░ąĮč¢čŚ Honda, Toyota, BMW, Mercedes-Benz čüčéą▓ąŠčĆąĖą╗ąĖ ą┐čĆąŠč鹊čéąĖą┐ąĖ ą╝ą░ą╣ą▒čāčéąĮč¢čģ čüąĄčĆč¢ą╣ąĮąĖčģ ą░ą▓čéč¢ą▓ąŠą║ ąĮą░ ą▓ąŠą┤ąĮąĄą▓ąŠ-ą║ąĖčüąĮąĄą▓ąĖčģ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéą░čģ. ąåąĮčłč¢ ą│č¢ą│ą░ąĮčéąĖ ą╝ą░čłąĖąĮąŠą▒čāą┤čāą▓ą░ąĮąĮčÅ ą┐čĆąŠčÅą▓ą╗čÅčÄčéčī ą░ą║čéąĖą▓ąĮąĖą╣ č¢ąĮč鹥čĆąĄčü ą┤ąŠ č鹥čģąĮąŠą╗ąŠą│č¢čŚ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓. ąĪčéą▓ąŠčĆąĄąĮąŠ ąĘą░čĆčÅą┤ąĮč¢ ą┐čĆąĖčüčéčĆąŠčŚ ąĮą░ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéą░čģ, ą┤ą╗čÅ ą╝ąŠą▒č¢ą╗čīąĮąĖčģ ą│ą░ą┤ąČąĄčéč¢ą▓, čÅą║č¢ ą┐čĆą░čåčÄčÄčéčī ąĮą░ ąŠą║ąĖčüąĮąĄąĮąĮč¢ ą╝ąĄčéą░ąĮąŠą╗čā.
ą¤čĆą░ą│ąĮąĄąĮąĮčÅ ąŠčéčĆąĖą╝ą░čéąĖ ą▓ąĖą│ąŠą┤čā č¢ čåč¢ą║ą░ą▓č¢čüčéčī ą┤ąŠ čüą┐čĆą░ą▓ąĖ, ą┐č¢ą┤čłč鹊ą▓čģčāčö ą┤ąŠčüą╗č¢ą┤ąČąĄąĮąĮčÅ ą▓ čüč乥čĆč¢ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓. ąöąŠčüą╗č¢ą┤ąĮąĖą║ąĖ ąĘą░ąĮčāčĆąĖą╗ąĖčüčī ą▓ ą▓ąĖčüąŠą║ąŠč鹥čģąĮąŠą╗ąŠą│č¢čćąĮč¢ ą┤ąŠčüą╗č¢ą┤ąČąĄąĮąĮčÅ, ą░ą╗ąĄ ą▓čüąĄ ą│ąĄąĮč¢ą░ą╗čīąĮąĄ – ą┐čĆąŠčüč鹊, č鹊ą╝čā, ą╝ąŠąČą╗ąĖą▓ąŠ, čĆąŠąĘą▓ŌĆÖčÅąĘą░ąĮąĮčÅ ą┐čĆąŠą▒ą╗ąĄą╝ ą┐ą░ą╗ąĖą▓ąĮąĖčģ ąĄą╗ąĄą╝ąĄąĮčéč¢ą▓ ą╗ąĄąČąĖčéčī ąĮą░ ą┐ąŠą▓ąĄčĆčģąĮč¢ ą┐ąĄčĆąĄą┤ ąŠčćąĖą╝ą░, ą┤ąŠčüčéą░čéąĮčīąŠ ą╗ąĖčłąĄ ą┐ąŠą│ą╗čÅąĮčāčéąĖ čüą▓č¢ąČąĖą╝ ą┐ąŠą│ą╗čÅą┤ąŠą╝…










