Між кількістю електрики, спожитої при електролізі, і масою речовини, що осаджується на електроді, існує залежність, відкрита в 1833 році англійським фізиком Фарадеєм.
Перший закон Фарадея
Маса речовини, яка виділяється на електроді під час електролізу, пропорційна кількості електрики, яка пройшла через розчин електроліту:
m = Ае * q
де m – маса речовини, г.; Аe – коефіцієнт пропорційності, званий електрохімічною еквівалентною масою, q – кількість електрики.
Якщо масу речовини виразити в грамах (г.), кількість електрики – в кулонах (Кл), то одиницею електрохімічної еквівалентної маси Аe буде г./Кл.
Оскільки кількість електрики q (Кл) є похідною сили електричного струму I (в амперах А) на тривалість електролізу τ(с), тобто q = Iτ, перший закон Фарадея можна представити у вигляді:
m = Ае * I * τ
Електрохімічна еквівалентна маса Ае є константа для кожної речовини в конкретній електрохімічної реакції.
Електрохімічна еквівалентна маса – це відношенням маси речовини, що виділилась при електролізі, до витраченої кількості електрики:
Ае = m / q
Приклад.
Електрохімічна еквівалентна маса срібла становить 1,11817e-3 г./Кл. Це означає, що при пропусканні через розчин солі, який містить іони Аg+ (які відновлюються до Аg0), електричного струму силою 1А тривалістю 1 с з розчину на катоді виділиться 1,11817e-3 г. срібла.
(Електрохімічна еквівалентна маса срібла раніше застосовувалася для визначення одиниці сили електричного струму – Ампер).
Фарадей встановив також взаємозв’язок між кількостями різних речовин, які виділяються на електродах за витратою однакової кількості електрики.
Другий закон Фарадея
Кількість двох різних речовин, які виділяються на електродах за витратою однакової кількості електрики, обернено пропорційні еквівалентним числам цих речовин:
n(A) / n(B) = z(B) / z(A)
де n(A) і n(B) – кількості речовин А і В, які виділяються на електродах (моль); z(A) і z(B) – еквівалентні числа речовин А і В у електрохімічних (окисно-відновних) реакціях.
Приклад.
Дві електролізні комірки, які містять відповідно CuSO4 і AgNO3, з’єднані послідовно.
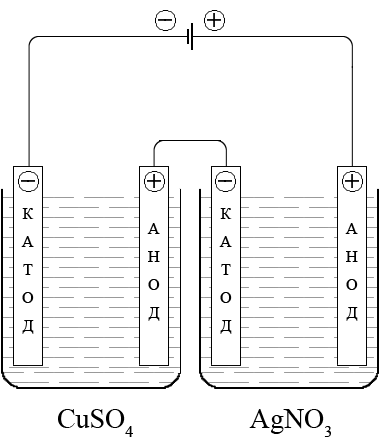
При протіканні електролізу на катодах будуть розряджатися іони Cu2+ (z = 2) і Ag+ (z = 1). Кількість міді, що виділилася за витратою кількості електрики, яка осаджує 1 моль срібла, складе:
n(Аg) / n(Cu) = z(Cu2+) / z(Аg+)
n(Cu) = n(Аg) * z(Аg+) / z(Сu2+) = 1 * 1 / 2 = 0,5 моль
Залежність, виражена у другому законі Фарадея, фізично пояснюється тим, що 1 моль (6,022e23) електронів розряджає
1 моль однозарядних іонів (Аg+ + e– = Аg0)
0,5 моль двозарядних іонів (Сu2+ + 2е– = Сu0)
1 / z моль z-зарядних іонів (Мz+ + zе– = М0)
Практично зручніше використовувати другий закон Фарадея, якщо ввести поняття еквівалентна кількість речовин neq.
При витраті однієї і тієї ж кількості електрики на електродах виділяються однакові еквівалентні кількості різних речовин:
neq(А) = neq(В)
У такому формулюванні другий закон Фарадея є наслідком закону еквівалентів для електрохімічних реакцій.
Приклад.
Еквівалентні кількості речовини міді і срібла, що виділяються в результаті електролізу (дивіться попередній приклад), однакові між собою:
neq(Ag) = n(Ag) * z(Ag+) = 1 * 1 = 1 моль
neq(Cu) = n(Cu) * z(Cu2+) = 0,5 * 2 = 1 моль
Другий закон Фарадея дозволяє перейти від кількостей речовин до їх масс (через молярні маси):
m(A) : m(B) = M(A) / z(А) : M(B) / z(B)
Приклад.
Потрібно визначити масу міді, що виділилась при електролізі розчину СuSO4, якщо відомо, що в послідовно з’єднаній електролізний комірці за витратою тієї ж кількості електрики виділилося 0,2157 г. срібла.
Маса складе:
m(Cu) = m(Ag) * (z(Ag+) * M(Cu)) / (z(Cu2+) * M(Ag)) = 0,2157 * ((1 * 63,546) / (2 * 107,868)) = 0,0636 г.
Виходячи з визначення еквівалентної маси, рівняння другого закону Фарадея можна записати у вигляді:
Meq = M / z, тоді m(A) / m(B) = Meq(А) / Meq(В)
Маси двох речовин, які виділяються на електродах при споживанні однакової кількості електрики, прямо пропорційні еквівалентним масам цих речовин
Приклад. Еквівалентні маси міді і срібла рівні:
Мeq(Cu) = M(Cu) / z(Cu2+) = 63,546/2 = 31,773 г./моль
Мeq(Ag) = M(Ag) / z(Ag+) = 107,868/1 = 107,868 г./моль
Відношення їх еквівалентних мас і відношення мас цих речовин (дивіться попередній приклад) повинні бути однакові:
Мeq(Cu) / Мeq(Ag) = 31,773 / 107,868 = 0,295
m(Cu) / m(Ag) = 0,0636 / 0,2157 = 0,295
З законів електролізу можна зробити наступне узагальнення: кількість електрики, необхідної для розрядки еквівалентної кількості будь-якої речовини в 1 моль, однакова; ця кількість електрики являє собою 1 моль елементарних електричних зарядів.
Постійна Фарадея – це кількість електрики, яку мають 1 моль елементарних електричних зарядів
F = 96484,56 Кл/моль
Числове значення постійної Фарадея (F) називають число Фарадея.
F = 96484,56 Кл/моль = 96484,56 А*с/моль = 26,8 А*год./моль
Выдношення постійної Фарадея до постійної Авогадро відповідає значенню елементарного електричного заряду:
F / NA = e– = 96484,56 Кл/моль / 6,022e23 моль-1 = 1,602189 Кл
Електрохімічна еквівалентна маса речовини Ае залежить від електрохімічної реакції і визначається як відношення:
Ае = М / (zF) = МeqIF
Приклад.
Для іонів Fе2+ і Fе3+ при їх відновленні до Fе0 (z = 2 і 3 відповідно) значення Ае наступні:
Ае(Fе2+) = M(Fe) / (z(Fe2+) * F) = 55,847 г./моль / (2 * 96484,56) = 2,894e-4 г./Кл
Ае(Fе3+) = M(Fe) / (z(Fe3+) * F) = 55,847 г./моль / (3 * 96484,56) = 1,929e-4 г./Кл
Об’єднавши всі попередні рівняння, можна записати:
m = МIτ / (zF)
З використанням цього рівняння проводяться всі розрахунки, засновані на законах електролізу.










