ąÆ ąŠčĆą│ą░ąĮąĖč湥čüą║ąĖčģ ą╝ąŠą╗ąĄą║čāą╗ą░čģ ą┤ą▓ąŠą╣ąĮčŗąĄ čüą▓čÅąĘąĖ C=C ą╝ąŠą│čāčé ą▒čŗčéčī:
- ą║čāą╝čāą╗ąĖčĆąŠą▓ą░ąĮąĮčŗąĄ, čé. ąĄ. čüą╗ąĄą┤čāčÄčēąĖą╝ąĖ ąĮąĄą┐ąŠčüčĆąĄą┤čüčéą▓ąĄąĮąĮąŠ ą┤čĆčāą│ ąĘą░ ą┤čĆčāą│ąŠą╝
ą┐ąĄąĮčéą░ą┤ąĖąĄąĮ-1,2 CH2=C=CH-CH2-CH3
- čüąŠą┐čĆčÅąČąĄąĮąĮčŗąĄ, čé. ąĄ. čĆą░ąĘą┤ąĄą╗ąĄąĮąĮčŗą╝ąĖ ąŠą┤ąĮąŠą╣ ąŠą┤ąĖąĮą░čĆąĮąŠą╣ čüą▓čÅąĘčīčÄ
ą┐ąĄąĮčéą░ą┤ąĖąĄąĮ-1,3 CH2=CH-CH=CH-CH3
- ąĖąĘąŠą╗ąĖčĆąŠą▓ą░ąĮąĮčŗąĄ, čé. ąĄ. čĆą░ąĘą┤ąĄą╗ąĄąĮąĮčŗą╝ąĖ ą┤ą▓čāą╝čÅ ąĖą╗ąĖ ąĮąĄčüą║ąŠą╗čīą║ąĖą╝ąĖ ąŠą┤ąĖąĮą░čĆąĮčŗą╝ąĖ čüą▓čÅąĘčÅą╝ąĖ
ą┐ąĄąĮčéą░ą┤ąĖąĄąĮ-1,4 CH2=CH-CH2-CH=CH2
ąóčĆąŠą╣ąĮčŗąĄ čüą▓čÅąĘąĖ CŌēĪC čéą░ą║ąČąĄ ą╝ąŠą│čāčé ąŠą║ą░ąĘą░čéčīčüčÅ čüąŠą┐čĆčÅąČąĄąĮąĮčŗą╝ąĖ ąĖą╗ąĖ ąĖąĘąŠą╗ąĖčĆąŠą▓ą░ąĮąĮčŗą╝ąĖ.
ąÆ ą╝ąŠą╗ąĄą║čāą╗ą░čģ čü čüąŠą┐čĆčÅąČąĄąĮąĮčŗą╝ąĖ čüą▓čÅąĘčÅą╝ąĖ ąĖčüčéąĖąĮąĮąŠąĄ čĆą░čüą┐čĆąĄą┤ąĄą╗ąĄąĮąĖąĄ 菹╗ąĄą║čéčĆąŠąĮąĮąŠą╣ ą┐ą╗ąŠčéąĮąŠčüčéąĖ čÅą▓ą╗čÅąĄčéčüčÅ ą┐čĆąŠą╝ąĄąČčāč鹊čćąĮčŗą╝ ą╝ąĄąČą┤čā čĆą░čüą┐čĆąĄą┤ąĄą╗ąĄąĮąĖčÅą╝ąĖ ą▓ ą┤ą▓čāčģ ąĖą╗ąĖ ąĮąĄčüą║ąŠą╗čīą║ąĖčģ ą║ą╗ą░čüčüąĖč湥čüą║ąĖčģ č乊čĆą╝čāą╗ą░čģ. ąŁč鹊 ą┐ąŠą╗ąŠąČąĄąĮąĖąĄ ą╗ąĄąČąĖčé ą▓ ąŠčüąĮąŠą▓ąĄ č鹥ąŠčĆąĖąĖ ą╝ąĄąĘąŠą╝ąĄčĆąĖąĖ, ąŠą┐ąĖčüčŗą▓ą░čÄčēąĄą╣ 菹╗ąĄą║čéčĆąŠąĮąĮąŠąĄ čüčéčĆąŠąĄąĮąĖąĄ čģąĖą╝ąĖč湥čüą║ąĖčģ čüąŠąĄą┤ąĖąĮąĄąĮąĖą╣ ąĖ čüąŠą┐čĆčÅąČąĄąĮąĮčŗą╝ąĖ čüą▓čÅąĘčÅą╝ąĖ.
ąĪąŠčüč鹊čÅąĮąĖąĄ ą╝ąĄąĘąŠą╝ąĄčĆąĖąĖ ą▓ąŠąĘą╝ąŠąČąĮąŠ, ąĄčüą╗ąĖ ąĖą╝ąĄčÄčéčüčÅ čüą╗ąĄą┤čāčÄčēąĖąĄ čüčéčĆčāą║čéčāčĆąĮčŗąĄ ą┐čĆąĄą┤ą┐ąŠčüčŗą╗ą║ąĖ:
- ąØą░ą╗ąĖčćąĖąĄ čüąŠą┐čĆčÅąČąĄąĮąĮčŗčģ ą║čĆą░čéąĮčŗčģ, ąŠčüąŠą▒ąĄąĮąĮąŠ ą┤ą▓ąŠą╣ąĮčŗčģ čüą▓čÅąĘąĄą╣ čāą│ą╗ąĄčĆąŠą┤-čāą│ą╗ąĄčĆąŠą┤ ąĖą╗ąĖ ą║čĆą░čéąĮčŗčģ čüą▓čÅąĘąĄą╣ čāą│ą╗ąĄčĆąŠą┤-ą│ąĄč鹥čĆąŠčŹą╗ąĄą╝ąĄąĮčé
ŌĆ”-C=C-C=CŌĆ”; ŌĆ”-C=C-C=O; ŌĆ”-C=C-CŌēĪN
- ąØą░ą╗ąĖčćąĖąĄ ą┤ą▓ąŠą╣ąĮąŠą╣ čüą▓čÅąĘąĖ, čüąŠą┐čĆčÅąČąĄąĮąĮąŠą╣ čü ąĮąĄą┐ąŠą┤ąĄą╗ąĄąĮąĮąŠą╣ 菹╗ąĄą║čéčĆąŠąĮąĮąŠą╣ ą┐ą░čĆąŠą╣ ą░č鹊ą╝ą░ ą│ąĄč鹥čĆąŠčŹą╗ąĄą╝ąĄąĮčéą░
ŌĆ”-C=C-Cl:
ą¤čĆąŠčüčéčĆą░ąĮčüčéą▓ąĄąĮąĮčŗą╝ čāčüą╗ąŠą▓ąĖąĄą╝ ą▓ąŠąĘąĮąĖą║ąĮąŠą▓ąĄąĮąĖčÅ ą╝ąĄąĘąŠą╝ąĄčĆąĖąĖ čÅą▓ą╗čÅąĄčéčüčÅ čĆą░čüą┐ąŠą╗ąŠąČąĄąĮąĖąĄ čüąŠąŠčéą▓ąĄčéčüčéą▓čāčÄčēąĄą╣ čüąĖčüč鹥ą╝čŗ čüą▓čÅąĘąĄą╣ ą▓ ąŠą┤ąĮąŠą╣ ą┐ą╗ąŠčüą║ąŠčüčéąĖ. ąĪčāčēąĮąŠčüčéčī ą╝ąĄąĘąŠą╝ąĄčĆąĖąĖ ąĘą░ą║ą╗čÄčćą░ąĄčéčüčÅ ą▓ č鹊ą╝, čćč鹊 ŽĆ-菹╗ąĄą║čéčĆąŠąĮčŗ čüąŠą┐čĆčÅąČąĄąĮąĮčŗčģ ą┤ą▓ąŠą╣ąĮčŗčģ čüą▓čÅąĘąĄą╣ ąĮą░čģąŠą┤čÅčéčüčÅ ąĮąĄ čüčéčĆąŠą│ąŠ ą╝ąĄąČą┤čā ą┤ą▓čāą║čĆą░čéąĮąŠ čüą▓čÅąĘą░ąĮąĮčŗą╝ąĖ ą░č鹊ą╝ą░ą╝ąĖ čāą│ą╗ąĄčĆąŠą┤ą░, ą░ ą▓ ąŠčéą╗ąĖčćąĖąĄ ąŠčé Žā-菹╗ąĄą║čéčĆąŠąĮąŠą▓ ą▒ąŠą╗ąĄąĄ ąĖą╗ąĖ ą╝ąĄąĮąĄąĄ čĆą░ą▓ąĮąŠą╝ąĄčĆąĮąŠ čĆą░čüą┐čĆąĄą┤ąĄą╗ąĄąĮčŗ ą┐ąŠ ą▓čüąĄą╣ ą╝ąĄąĘąŠą╝ąĄčĆąĮąŠą╣ čüąĖčüč鹥ą╝ąĄ čüą▓čÅąĘąĄą╣, čé.ąĄ. ą┤ąĄą╗ąŠą║ą░ą╗ąĖąĘąŠą▓ą░ąĮčŗ. ą¤čĆąĖ čéą░ą║ąŠą╝ čĆą░čüą┐čĆąĄą┤ąĄą╗ąĄąĮąĖąĖ ą▓čŗčüą▓ąŠą▒ąŠąČą┤ą░ąĄčéčüčÅ čŹąĮąĄčĆą│ąĖčÅ ą╝ąĄąĘąŠą╝ąĄčĆąĖąĘą░čåąĖąĖ, ą░ čüą╗ąĄą┤ąŠą▓ą░č鹥ą╗čīąĮąŠ, ą╝ąĄąĘąŠą╝ąĄčĆąĮą░čÅ čüąĖčüč鹥ą╝ą░ ą┤ąŠą╗ąČąĮą░ ą┐čĆąĖąŠą▒čĆąĄčüčéąĖ ą▒ąŠą╗čīčłčāčÄ čāčüč鹊ą╣čćąĖą▓ąŠčüčéčī.
ą¤čĆąĖą╝ąĄčĆ. ą¤ąŠą╗čāčćąĖčéčī čüąĖą╗čīąĮąŠ ąĮąĄąĮą░čüčŗčēąĄąĮąĮčŗą╣ čåąĖą║ą╗ čåąĖą║ą╗ąŠą│ąĄą║čüą░čéčĆąĖąĄąĮ, ą╝ąŠą╗ąĄą║čāą╗čŗ ą║ąŠč鹊čĆąŠą│ąŠ čüąŠą┤ąĄčƹȹ░ą╗ąĖ ą▒čŗ ą║ąŠą╗čīčåąĄą▓čāčÄ čüąĖčüč鹥ą╝čā čü čéčĆąĄą╝čÅ čüąŠą┐čĆčÅąČąĄąĮąĮčŗą╝ąĖ ą┤ą▓ąŠą╣ąĮčŗą╝ąĖ čüą▓čÅąĘčÅą╝ąĖ (1 ąĖ 3 č乊čĆą╝čāą╗čŗ), ąĮąĄ čāą┤ą░ąĄčéčüčÅ, ą▓ ą┤ąĄą╣čüčéą▓ąĖč鹥ą╗čīąĮąŠčüčéąĖ ąŠą▒čĆą░ąĘčāąĄčéčüčÅ ąŠčéąĮąŠčüąĖč鹥ą╗čīąĮąŠ ą▒ąŠą╗ąĄąĄ ąĮą░čüčŗčēąĄąĮąĮčŗą╣ ąĖ ą▒ąŠą╗ąĄąĄ čāčüč鹊ą╣čćąĖą▓čŗą╣ ą▒ąĄąĮąĘąŠą╗ (2 č乊čĆą╝čāą╗ą░) – čĆąŠą┤ąŠąĮą░čćą░ą╗čīąĮąĖą║ ą░čĆąŠą╝ą░čéąĖč湥čüą║ąĖčģ čüąŠąĄą┤ąĖąĮąĄąĮąĖą╣. ą©ąĄčüčéčī ŽĆ-菹╗ąĄą║čéčĆąŠąĮąŠą▓ čåąĖą║ą╗ąŠą│ąĄą║čüą░čéčĆąĖąĄąĮą░ ą┐čĆąĖ čüąĖą╗čīąĮąŠą╝ ą▓čŗąĖą│čĆčŗčłąĄ 菹ĮąĄčĆą│ąĖąĖ čĆą░ą▓ąĮąŠą╝ąĄčĆąĮąŠ čĆą░čüą┐čĆąĄą┤ąĄą╗čÅčÄčéčüčÅ (ą┤ąĄą╗ąŠą║ą░ą╗ąĖąĘčāčÄčéčüčÅ) ą┐ąŠ ą▓čüąĄą╣ ą║ąŠą╗čīčåąĄą▓ąŠą╣ čüąĖčüč鹥ą╝ąĄ (čüą▓čÅąĘčŗą▓ą░čÄčēąĖąĄ ą╝ąŠą╗ąĄą║čāą╗čÅčĆąĮčŗąĄ ąŠčĆą▒ąĖčéą░ą╗ąĖ ŽĆ-菹╗ąĄą║čéčĆąŠąĮąŠą▓ ą┐čĆąĄą┤čüčéą░ą▓ą╗čÅčÄčé čüąŠą▒ąŠą╣ ą┐čĆąŠčüčéčĆą░ąĮčüčéą▓ąĄąĮąĮąŠąĄ ą║ąŠą╗čīčåąŠ, čĆą░čüą┐ąŠą╗ąŠąČąĄąĮąĮąŠąĄ ąĮą░ą┤ ąĖ ą┐ąŠą┤ ą┐ą╗ąŠčüą║ąŠčüčéčīčÄ ą╝ąŠą╗ąĄą║čāą╗čŗ)
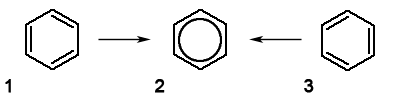
ąóą░ą║ąĖą╝ ąŠą▒čĆą░ąĘąŠą╝, ą▓ąŠąĘąĮąĖą║ą░ąĄčé ą╝ąĄąĘąŠą╝ąĄčĆąĮą░čÅ (ą▓ ą┤ą░ąĮąĮąŠą╝ čüą╗čāčćą░ąĄ – ą░čĆąŠą╝ą░čéąĖč湥čüą║ą░čÅ) čüąĖčüč鹥ą╝ą░ čüą▓čÅąĘąĄą╣. ąÆ čåąĖą║ą╗ąŠąŠą║čéą░č鹥čéčĆą░ąĄąĮąĄ (ąĘą░ą╝ą║ąĮčāčéą░čÅ čåąĖą║ą╗ąĖč湥čüą║ą░čÅ čüąĖčüč鹥ą╝ą░ čü č湥čéčŗčĆčīą╝čÅ ą┤ą▓ąŠą╣ąĮčŗą╝ąĖ čüą▓čÅąĘčÅą╝ąĖ) ą╝ąĄąĘąŠą╝ąĄčĆąĖąĖ ą▒čŗčéčī ąĮąĄ ą╝ąŠąČąĄčé, čéą░ą║ ą║ą░ą║ ą╝ąŠą╗ąĄą║čāą╗ą░ ąĮąĄ čÅą▓ą╗čÅąĄčéčüčÅ ą┐ą╗ąŠčüą║ąŠą╣, ą░ ąĖą╝ąĄąĄčé ą║ąŠąĮč乊čĆą╝ą░čåąĖčÄ ŌĆ£ą▓ą░ąĮąĮčŗŌĆØ. ąöąĄą╣čüčéą▓ąĖč鹥ą╗čīąĮąŠąĄ čüčéčĆąŠąĄąĮąĖąĄ ą▒ąĄąĮąĘąŠą╗ą░ (2 č乊čĆą╝čāą╗ą░) ą┐čĆąŠą╝ąĄąČčāč鹊čćąĮąŠ ą╝ąĄąČą┤čā čüčéčĆąŠąĄąĮąĖąĄą╝ ą┐ąŠą║ą░ąĘą░ąĮąĮčŗą╝ 1 ąĖ 3 č乊čĆą╝čāą╗ą░ą╝ąĖ. ąÜąŠąĮąĄčćąĮąŠ, ą▓ąŠ ą╝ąĮąŠą│ąĖčģ čüą╗čāčćą░čÅčģ ą╝ąŠąČąĮąŠ ą┐ąŠą╗čīąĘąŠą▓ą░čéčīčüčÅ ą║ą╗ą░čüčüąĖč湥čüą║ąĖą╝ (čéčĆą░ą┤ąĖčåąĖąŠąĮąĮčŗą╝) ąĖąĘąŠą▒čĆą░ąČąĄąĮąĖąĄą╝ ą╝ąŠą╗ąĄą║čāą╗čŗ ą▒ąĄąĮąĘąŠą╗ą░ ą▓ ą▓ąĖą┤ąĄ č乊čĆą╝čāą╗čŗ 1 ąĖą╗ąĖ čĆą░ą▓ąĮąŠąĘąĮą░čćąĮąŠą╣ ąĄą╣ č乊čĆą╝čāą╗čŗ 3, ą▓ą╝ąĄčüč鹊 čĆąĄą░ą╗čīąĮąŠą╣ č乊čĆą╝čāą╗čŗ 2. ąóą░ą║ąĖąĄ č乊čĆą╝čāą╗čŗ, ą║ą░ą║ 1 ąĖ 3 ą┤ą╗čÅ ą▒ąĄąĮąĘąŠą╗ą░, ą║ąŠč鹊čĆčŗąĄ ą┐čĆąĖ ąĮą░ą╗ąŠąČąĄąĮąĖąĖ ą┐čĆąĖą▓ąŠą┤čÅčé ą║ ą╝ąĄąĘąŠą╝ąĄčĆąĮąŠą╣ čüčéčĆčāą║čéčāčĆąĄ, ąĮą░ąĘčŗą▓ą░čÄčéčüčÅ ą│čĆą░ąĮąĖčćąĮčŗąĄ č乊čĆą╝čāą╗čŗ. ą£ąĄąĘąŠą╝ąĄčĆąĮčāčÄ čüčéčĆčāą║čéčāčĆčā ąŠą▒čŗčćąĮąŠ ąĖąĘąŠą▒čĆą░ąČą░čÄčé ą┤ą▓čāą╝čÅ ą│čĆą░ąĮąĖčćąĮčŗą╝ąĖ č乊čĆą╝čāą╗ą░ą╝ąĖ, čüąŠąĄą┤ąĖąĮąĄąĮąĮčŗą╝ąĖ ą┤ą▓čāčüč鹊čĆąŠąĮąĮąĄą╣ čüčéčĆąĄą╗ą║ąŠą╣ (Ōåö):
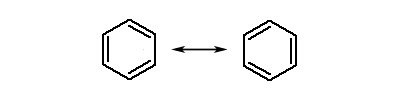
ą£ąĄąĘąŠą╝ąĄčĆąĮčāčÄ čüčéčĆąĄą╗ą║čā (Ōåö) ąĮąĄą╗čīąĘčÅ ąĘą░ą╝ąĄąĮčÅčéčī ąĮą░ ąĘąĮą░ą║ ąŠą▒čĆą░čéąĖą╝ąŠčüčéąĖ (Ōćä). ąÆ ą╝ąĄąĘąŠą╝ąĄčĆąĮąŠą╣ čüąĖčüč鹥ą╝ąĄ čüą▓čÅąĘąĄą╣ ąĮąĄčé čģąĖą╝ąĖč湥čüą║ąŠą│ąŠ čĆą░ą▓ąĮąŠą▓ąĄčüąĖčÅ ą╝ąĄąČą┤čā čĆą░ąĘą╗ąĖčćąĮčŗą╝ąĖ ą╝ąŠą╗ąĄą║čāą╗ą░ą╝ąĖ, ąĖ ąŠąĮą░ čüčāčēąĄčüčéą▓čāąĄčé č鹊ą╗čīą║ąŠ ą║ą░ą║ ąŠą┤ąĖąĮ ą▓ąĖą┤ ą╝ąŠą╗ąĄą║čāą╗, čüčéčĆąŠąĄąĮąĖąĄ ą║ąŠč鹊čĆčŗčģ ąŠą┤ąĖąĮą░ą║ąŠą▓ąŠ ąĖ ąĮą░čģąŠą┤ąĖčéčüčÅ ą╝ąĄąČą┤čā čāą║ą░ąĘą░ąĮąĮčŗą╝ąĖ ą│čĆą░ąĮąĖčćąĮčŗą╝ąĖ č乊čĆą╝čāą╗ą░ą╝ąĖ.
ąōčĆą░ąĮąĖčćąĮčŗąĄ č乊čĆą╝čāą╗čŗ ą╝ąŠą│čāčé ą▒čŗčéčī ąĘą░ą┐ąĖčüą░ąĮčŗ ą▓ č乊čĆą╝ąĄ, ąŠč鹊ą▒čĆą░ąČą░čÄčēąĄą╣ ą┐ąŠą╗čÅčĆąĮąŠčüčéčī ą╝ąŠą╗ąĄą║čāą╗čŗ. ąØą░ą┐čĆąĖą╝ąĄčĆ, ą┤ąĄą╣čüčéą▓ąĖč鹥ą╗čīąĮąŠąĄ čüčéčĆąŠąĄąĮąĖąĄ ą▓ąĖąĮąĖą╗čģą╗ąŠčĆąĖą┤ą░ (č乊čĆą╝čāą╗ą░ 6) čüąŠąŠčéą▓ąĄčéčüčéą▓čāąĄčé čüąŠčüč鹊čÅąĮąĖčÄ ą╝ąŠą╗ąĄą║čāą╗čŗ, ą┐čĆąŠą╝ąĄąČčāč鹊čćąĮąŠą╝čā ą╝ąĄąČą┤čā ąĮąĄą┐ąŠą╗čÅčĆąĮąŠą╣ ą│čĆą░ąĮąĖčćąĮąŠą╣ č乊čĆą╝čāą╗ąŠą╣ 4 ąĖ ą┐ąŠą╗čÅčĆąĮąŠą╣ ą│čĆą░ąĮąĖčćąĮąŠą╣ č乊čĆą╝čāą╗ąŠą╣ 5:
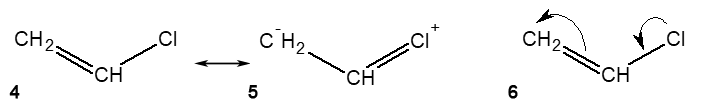
ą¤ąŠą╗čÅčĆąĮą░čÅ ą│čĆą░ąĮąĖčćąĮą░čÅ č乊čĆą╝čāą╗ą░ 5 ą▓ąĖąĮąĖą╗čģą╗ąŠčĆąĖą┤ą░ čüą╗ąĄą┤čāąĄčé ąĖąĘ ąĮąĄą┐ąŠą╗čÅčĆąĮąŠą╣ č乊čĆą╝čāą╗čŗ 4: ą░č鹊ą╝ čģą╗ąŠčĆą░ ą┐ąĄčĆąĄą┤ą░ąĄčé ąŠą┤ąĖąĮ 菹╗ąĄą║čéčĆąŠąĮ ąĮą░ čüąŠčüąĄą┤ąĮąĖą╣ ą░č鹊ą╝ čāą│ą╗ąĄčĆąŠą┤ą░ ąĖ č鹥ą╝ čüą░ą╝čŗą╝ ą┤ąĄą╗ą░ąĄčé čüą▓ąŠčÄ ąĮąĄą┐ąŠą┤ąĄą╗ąĄąĮąĮčāčÄ čŹą╗ąĄą║čéčĆąŠąĮąĮčāčÄ ą┐ą░čĆčā čüą▓čÅąĘčŗą▓ą░čÄčēąĄą╣, ą┐čĆąĖ čŹč鹊ą╝ ą░č鹊ą╝ čģą╗ąŠčĆą░ ą┐čĆąĖąŠą▒čĆąĄčéą░ąĄčé ą┐ąŠą╗ąŠąČąĖč鹥ą╗čīąĮčŗą╣ ąĘą░čĆčÅą┤. ą¤ąĄčĆąĄą┤ą░čćą░ 菹╗ąĄą║čéčĆąŠąĮą░ (ą┐ąŠą╗ąŠąČąĖč鹥ą╗čīąĮčŗą╣ ą╝ąĄąĘąŠą╝ąĄčĆąĮčŗą╣ čŹčäč乥ą║čé) ą┐čĆąŠčģąŠą┤ąĖčé č湥čĆąĄąĘ čüąŠčüąĄą┤ąĮąĖą╣ (čü ą░č鹊ą╝ąŠą╝ čģą╗ąŠčĆą░) ą░č鹊ą╝ čāą│ą╗ąĄčĆąŠą┤ą░ ą║ ą║ąŠąĮčåąĄą▓ąŠą╝čā ą░č鹊ą╝čā čāą│ą╗ąĄčĆąŠą┤ą░, ą║ąŠč鹊čĆčŗą╣ ą┐čĆąĖąŠą▒čĆąĄčéą░ąĄčé ąŠčéčĆąĖčåą░č鹥ą╗čīąĮčŗą╣ ąĘą░čĆčÅą┤. ąóą░ą║ąĖąĄ čüą┤ą▓ąĖą│ąĖ (菹╗ąĄą║čéčĆąŠąĮąĮčŗąĄ čüą╝ąĄčēąĄąĮąĖčÅ) ą┐ąŠą║ą░ąĘą░ąĮčŗ ąĖąĘąŠą│ąĮčāčéčŗą╝ąĖ čüčéčĆąĄą╗ą║ą░ą╝ąĖ ą▓ čĆąĄą░ą╗čīąĮąŠą╣ č乊čĆą╝čāą╗ąĄ 6 ą┤ą╗čÅ ą▓ąĖąĮąĖą╗čģą╗ąŠčĆąĖą┤ą░.
ąÆ ą▒čāčéą░ą┤ąĖąĄąĮąĄ-1,3 č湥čéčŗčĆąĄ ŽĆ-菹╗ąĄą║čéčĆąŠąĮą░ ąŠą▒ąĄąĖčģ ą┤ą▓ąŠą╣ąĮčŗčģ čüą▓čÅąĘąĄą╣ čĆą░čüą┐čĆąĄą┤ąĄą╗ąĄąĮčŗ ą┐ąŠ ąŠą▒čēąĄą╣ čüąŠą┐čĆčÅąČąĄąĮąĮąŠą╣ čüąĖčüč鹥ą╝ąĄ čüą▓čÅąĘąĄą╣. ąĀąĄą░ą╗čīąĮąŠąĄ čüąŠčüč鹊čÅąĮąĖąĄ čüą▓čÅąĘąĄą╣ ąŠą┐ąĖčüčŗą▓ą░ąĄčéčüčÅ ąĮą░ą╗ąŠąČąĄąĮąĖąĄą╝ čéčĆąĄčģ ą│čĆą░ąĮąĖčćąĮčŗčģ č乊čĆą╝čāą╗
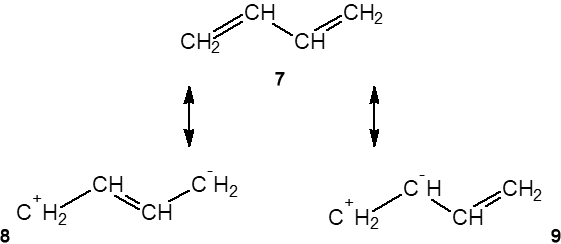
ąĖąĘ ą║ąŠč鹊čĆčŗčģ ąĮąĄą┐ąŠą╗čÅčĆąĮą░čÅ č乊čĆą╝čāą╗ą░ 7 čüčćąĖčéą░ąĄčéčüčÅ ą║ą╗ą░čüčüąĖč湥čüą║ąŠą╣ ą│čĆą░čäąĖč湥čüą║ąŠą╣ č乊čĆą╝čāą╗ąŠą╣ ą▒čāčéą░ą┤ąĖąĄąĮą░-1,3.
ąöą╗čÅ ąĮąĖčéčĆąŠą│čĆčāą┐ą┐čŗ NO2 ąĖ ą║ą░čĆą▒ąŠą║čüąĖą╗ą░čé-ąĖąŠąĮą░ COO– ą│čĆą░ąĮąĖčćąĮčŗą╝ąĖ č乊čĆą╝čāą╗ą░ą╝ąĖ ą▒čāą┤čāčé:
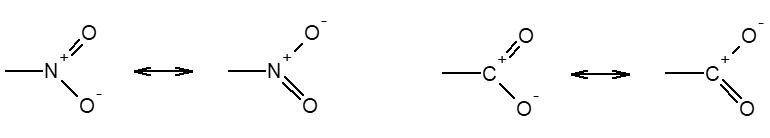
ą¤čĆąĖ čģąĖą╝ąĖč湥čüą║ąĖčģ čĆąĄą░ą║čåąĖčÅčģ ą╝ąĄąĘąŠą╝ąĄčĆąĮąŠąĄ (čé. ąĄ. ą┤ąĄą╣čüčéą▓ąĖč鹥ą╗čīąĮąŠąĄ) čüčéčĆąŠąĄąĮąĖąĄ ą┐ąŠą┤ ą▓ą╗ąĖčÅąĮąĖąĄą╝ čĆąĄą░ą│ąĄąĮčéą░-ą┐ą░čĆčéąĮąĄčĆą░ ą╝ąŠąČąĄčé ą┐čĆąĖą▒ą╗ąĖąČą░čéčīčüčÅ ą║ ąŠą┤ąĮąŠą╣ ąĖąĘ ą│čĆą░ąĮąĖčćąĮčŗčģ č乊čĆą╝čāą╗.










